Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương pháp điều chế Clo trong phòng thí nghiệm:
+Đun nóng nhẹ dung dịch axit clorua đậm đặc với chất có khả năng oxy hóa mạnh như mangan dioxit (MnO2).-->dùng trong hòng thí nghiệm
+ dùng một số chất oxy hóa khác như kali pemanganat (KMnO4), Kali Clorat (KClO3), Clorua vôi (CaOCl2)-->dùng trong phòng thí nghiệm
+ tiến hành điện phân muối Natri Clorua bằng điện phân nóng chảy theo phương trình phản ứng Hoặc điện phân có màng ngăn dung dịch muối halogenua (natri clorua)--->trong công nghiệp
b) nước Javen
2NaOH+Cl2--->NaClO+NaCl+H2O
Clorua vôi
Ca(OH)2+Cl--->CaOCl2+H2O
Kaliclorat
2KCl+3O2--->2KClO3

Điều chế oxi:
- Trong phòng thí nghiệm, oxi được điều chế bằng cách phân hủy những hợp chất giàu Oxi và ít bên với nhiệt như KMnO4, KClO3, ...
2KMnO4 → K2MnO4 + MnO2 + O2
2KClO3 → 2KCl + 3O2
- Trong công nghiệp:
a) Từ không khí: Không khí sau khi đã loại bỏ hết hơi nước, khí CO2, được hóa lỏng dưới áp suất 200 atm đồng thời hạ thấp nhiệt độ. Chưng cất phân đoạn không khí lỏng, thu được oxi lỏng. Oxi lỏng được vận chuyển trong những bình thép có thể tích 100 lít dưới áp suất 150atm.
b) Từ nước. Điện phân nước: 2H2O
Người ta không áp dụng phương pháp phòng thí nghiệm cho phòng thí nghiệm vì trong phòng thí nghiệm chỉ điều chế lượng nhỏ oxi, còn công nghiệp cần một lượng lớn giá thảnh rẻ.

a) Nước Gia-ven:
\(2NaCl+H_2O\underrightarrow{đpkmn}NaCl+NaClO+H_2\)
b) Clorua vôi
\(2NaCl+2H_2O\underrightarrow{đpcmn}2NaOH+H_2+Cl_2\)
\(Cl_2+Ca\left(OH\right)_2\rightarrow CaOCl_2+H_2O\)
c)
\(6KOH+3Cl_2\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)

Phương trình hóa học của phản ứng điều chế hidro clorua
2NaCltinh thể + H2SO4 đđ -to→ Na2SO4 + 2HCl
2KCl + 2H2O -đpdd có m.ngăn→ 2KOH + H2 + Cl2
H2 + Cl2 -as→ 2HCl.

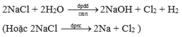
- Sản xuất clo trong CN:
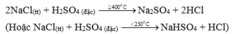
- Điều chế HCl trong PTN theo pp sunfat:

KCl(rắn)+H2O--->dung dịch KCl, 2KCl+2H2O----điện phân dung dịch-->2 KOH+H2+Cl2(1).Từ pt(1)ta thu được H2 và Cl2=>ta có pt:H2+Cl2-ánh sáng------>2HCl.chúc bạn học giỏi nhé.

(đặc) ---
--->
Có thêm nước để điều chế acid clohidric chứ  dẫn khí thu được qua nước
dẫn khí thu được qua nước
![]()

Điều chế axit HCl từ NaCl, H2SO4 đặc, H2O:
NaCl + H2SO4 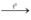 NaHSO4 + HCl
NaHSO4 + HCl
Hấp thụ khí hidro clorua vào nước được dung dịch axit HCl.
- Từ axit HCl và MnO2 điều chế Cl2:
MnO2 + 4HCl → MnCl2 + 2H2O + Cl2
- Từ Cl2 và dung dịch NaOH điều chế nước Gia – ven.
Cl2 + 2NaOH → NaCl + NaClO + H2O.
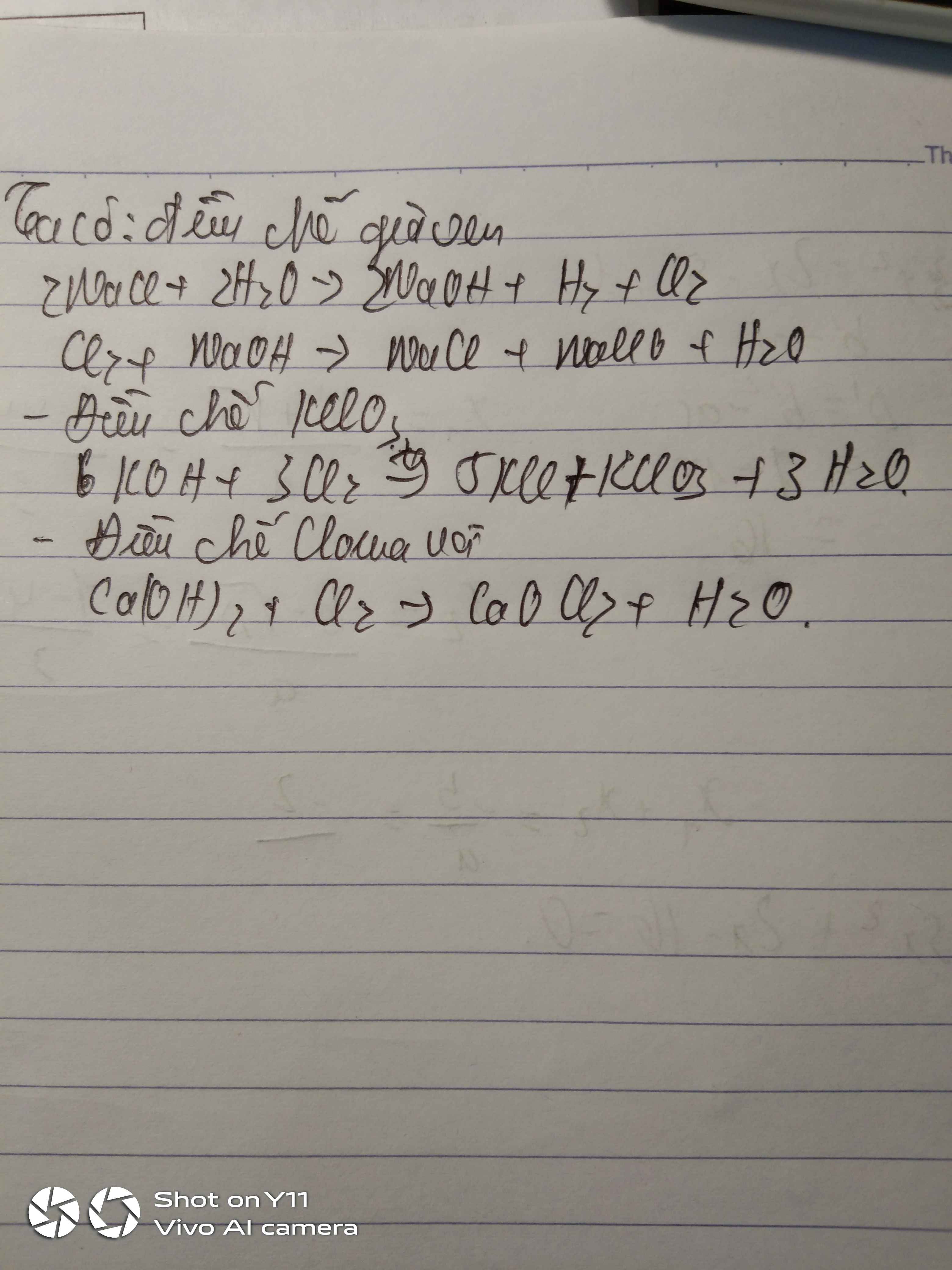
* Điều chế clo:
+ Trong phòng thí nghiệm: Sử dụng HCl đặc tác dụng với chất oxi hóa mạnh.
VD: \(16HCl+2KMnO_4\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(MnO_2+4HCl\rightarrow MnCL_2+Cl_2+2H_2O\)
\(K_2Cr_2O_7+14HCl\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
+ Trong công nghiệp: Điện phân dung dịch có màng ngăn NaCl
\(2NaCl+2H_2O\xrightarrow[cmn]{Đpdd}2NaOH+H_2+Cl_2\)
* Điều chế hiđro clorua:
+ Trong phòng thí nghiệm:
\(NaCl_{tt}+H_2SO_{4_đ}\underrightarrow{< 250^oC}NaHSO_4+HCl\uparrow\)
+ Trong công nghiệp:
\(2NaCl+2H_2O\xrightarrow[cmn]{Đpdd}2NaOH+Cl_2+H_2\)
\(H_2+Cl_2\rightarrow2HCl\)
Bạn tham khảo nhé!