Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B

Đáp án A
Bảo toàn e : ne = 2nCu + 3nAl = nNO3 muối = 3nNO = 0,09 mol
=> mmuối = mKL + mNO3 muối = 7,77g

Ta có nNO= 0,15 mol
QT nhận e:
NO3-+ 3e+ 4H+ → NO+ 2H2O
Ta có nNO3- trong muối= ne= 3.nNO= 3.0,15= 0,45 mol
→mmuối nitrat= mkim loại+ mNO3-trong muối= m+ 0,45.62= m+27,9 (gam)
Đáp án D






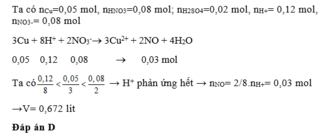

nCu=0,045 mol
nHNO3= 0,6* 0,1=0,06 mol. Suy ra nNO3= 0,06 mol
nH2SO4= 0,1* 0,3= 0,03 mol. Suy ra nH= nHNO3+ 2nH2So4= 0,12
3Cu + 8 H + 2NO3--- 3 Cu2+ +2 NO+ 4H2O
0,045 0,12 0,03 0,03
Suy ra nNO3 trong muối= 0,06-0,03=0,03 mol
nSO4 trong muối= nh2so4= 0,03
khi đó m muối= 2.88+ 0.03*96+ 0,03*62=7,62 gam