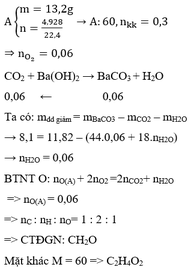Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chất A chứa C, H, O khi đốt cháy sẽ sinh ra CO 2 và H 2 O . Khi qua bình 1 đựng H 2 SO 4 đặc thì H 2 O bị hấp thụ. Vậy khối lượng H 2 O là 1,8 gam. Qua bình 2 có phản ứng :
Ca OH 2 + CO 2 → CaCO 3 ↓+ H 2 O
Theo phương trình : n CO 2 = n CaCO 3 = 10/100 = 0,1 mol
Vậy khối lượng cacbon có trong 3 gam A là 0,1 x 12 = 1,2 (gam).
Khối lượng hiđro có trong 3 gam A là 0,1 x 2 = 0,2 (gam).
Khối lượng oxi có trong 3 gam A là 3 - 1,2 - 0,2 = 1,6 (gam).
Gọi công thức phân tử của A là C x H y O z
Ta có :
60 gam A → 12x gam C → y g H → 16z gam O
3 gam → 1,2 gam → 0,2 gam → 1,6 gam
x = 1,2x60/36 = 2; y = 60x0,2/3 = 4
z = 1,6x60/48 = 2
→ Công thức phân tử của A là C 2 H 4 O 2

a.

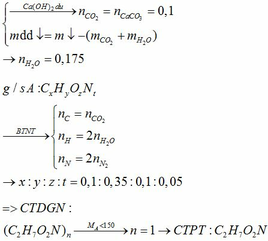
b.
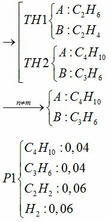
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)

a, \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)=n_C\)
⇒ mC + mH = 0,2.12 + 0,4.1 = 2,8 (g) < mA
→ A gồm C, H và O.
⇒ mO = 6 - 2,8 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,4:0,2 = 1:2:1
→ CTPT của A có dạng (CH2O)n
Không biết đề có cho thêm dữ kiện liên quan đến MA không bạn nhỉ?

Ta có: \(\left\{{}\begin{matrix}m_{H_2O}=5,4\left(g\right)\\m_{CO_2}=6,6\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\\n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_H=2n_{H_2O}=0,6\left(mol\right)\\n_C=n_{CO_2}=0,15\left(mol\right)\end{matrix}\right.\)
`=> m_C + m_H = 0,15.12 + 0,6 = 2,4 (g) = m_A`
`=> A` không chứa O
\(M_A=0,5.32=16\left(g/mol\right)\)
Ta có: \(n_C:n_H=0,15:0,6=1:4\)
`=>` CTPT của A có dạng \(\left(CH_4\right)_n\)
\(\Rightarrow n=\dfrac{16}{16}=1\)
Vậy A là CH4