Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=0,1 mol
nO2=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g
2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=6,5/65=0,1 mol
n O2=0,8/32=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g

C1: Độ tan của KNO3 ở 20oC là:
S KNO3= 60/190*100= 31.57g
C2:
nFe= 25.2/56=0.45 mol
3Fe + 2O2 -to-> Fe3O4
0.45___0.3
VO2= 0.3*22.4=6.72l
2KClO3 -to-> 2KCl + 3O2
0.2________________0.3
mKClO3= 0.2*122.5=24.5g
Câu 1:
\(S^{20^0C}_{KNO_3}=\frac{60}{190}.100=31,57\left(g\right)\)
Câu 2:
a) \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\left(1\right)\)
b) \(n_{Fe}=\frac{25,2}{56}=0,45\left(mol\right)\)
Theo PTHH (1): \(n_{Fe}:n_{O_2}=3:2\)
\(\Rightarrow n_{O_2}=n_{Fe}.\frac{2}{3}=0,45.\frac{2}{3}=0,3\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)
c) PTHH: \(2KClO_3\underrightarrow{t^0}2KCl+3O_2\left(2\right)\)
Theo PTHH (2): \(n_{O_2}:n_{KClO_3}=3:2\)
\(\Rightarrow n_{KClO_3}=n_{O_2}.\frac{2}{3}=0,3.\frac{2}{3}=0,2\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=0,2.122,5=24,5\left(g\right)\)

Bài 1:
a) nFe = \(\frac{25,2}{56}= 0,45\) mol
Pt: 3Fe + ..2O2 --to--> Fe3O4
0,45 mol-> 0,3 mol
VO2 = 0,3 . 22,4 = 6,72 (lít)
b) Pt: CH4 + ....2O2 --to--> CO2 + 2H2O
......0,15 mol<-0,3 mol
mCH4 = 0,15 . 16 = 2,4 (g)
Bài 2:
a) nAl = \(\frac{5,4}{27}= 0,2\) mol
Pt: 4Al + 3O2 --to--> 2Al2O3
0,2 mol->0,15 mol-->0,1 mol
mAl2O3 = 0,1 . 102 = 10,2 (g)
b) VO2 = 0,15 . 22,4= 3,36 (lít)
Mà: VO2 = 20%Vkk = 0,2Vkk
=> Vkk = \(\frac{VO2}{0,2}=\frac{3,36}{0,2}=16,8 \) (lít)

\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)ZnO\)
1 1/2 1 (mol)
0,3 0,15 0,3 ( mol )
PƯ trên thuộc loại phản ứng hóa hợp
\(m_{ZnO}=n_{ZnO}.M_{ZnO}=0,3.81=24,3g\)
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)

Câu 1:
Oxit là hợp chất có 2 nguyên tố, trong đó có 1 nguyên tố oxi.
Vd: BaO, Na2O, K2O, SO2,...
Câu 2:
\(a,2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(b,CaCO_3\underrightarrow{t^o}CaO+CO_2\)
\(c,2SO_2+O_2\underrightarrow{t^o}2SO_3\)
\(d,2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(e,C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Câu 3:
Oxit axit:
BaO: bari oxit
NO2: nito đioxit
Oxit bazo:
Fe3O4: oxit sắt từ
KMnO4: kali pemanganat
HgO: thủy ngân (II) oxit
ZnCl2? liên quan
Câu 4:
\(KSO_4\rightarrow K_2SO_4\)
\(MgCl\rightarrow MgCl_2\)
Câu 6:
a) \(n_{Fe}=\frac{33,6}{56}=0,6\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,6____0,4____0,2(mol)
b) \(V_{O_2}=0,4.22,4=8,96\left(l\right)\)
c) \(m_{Fe_3O_4}=0,2.232=46,4\left(g\right)\)
Chúc bạn học tốt

Bài 1:
+ Oxit axit
SiO2:Silic đioxit
SO2: Lưu huỳnh đioxit
NO: Nito oxit
+ Oxit bazo
Fe2O3: Sắt (III) oxit
Cu2O: Đồng (I) oxit
Ag2O: Bạc(I) oxit
Bài 2:
a/ 2KMnO4 → K2MnO4 + MnO2 + O2 → Phản ứng phân hủy
b/ Na2O + H2O → 2NaOH → Phản ứng hóa hợp
c/ 2Al + 3Cl2 → 2AlCl3 → Phản ứng hóa hợp
d/ 2Fe(OH)3 → Fe2O3 + 3H2O → Phản ứng phân hủy
Bài 3:
\(3Fe+2O_2\rightarrow Fe_3O_4\)
2,25___1,5___________
\(n_{Fe}=\frac{126}{56}=2,25\left(mol\right)\)
\(\Rightarrow V_{O2}=1,5.22,4=33,6\left(l\right)\)
\(2KClO_3\rightarrow2KCl+3O_2\)
1_________________1,5
\(\Rightarrow m_{KClO3}=1.\left(39+35,5+16.3\right)=122,5\left(g\right)\)

nFe= 2,8/56=0,05(mol)
PTHH: 3Fe+2O2-> Fe3O4
0,05 0,003 0,0167
a) mFe3O4= 0,0167. 232=3,8744(g)
b) Vo2 = 0,003.22,4=0,0672(l)
Ta có : nFe=2,8/56=0,05 mol
3Fe+2O2--->Fe3O4 (1)
a) theo pt (1) nFe3O4=1/3nFe=1/60 mol
=> mFe3O4=1/60 . MFe3O4 =58/15 gam
b) nO2 =2/3 nFe=0,05 .2/3=1/30 mol
=> VO2=1/30 .22,4=0,7467 lít
c) Vkhông khí=5. VO2=3,73 lít.
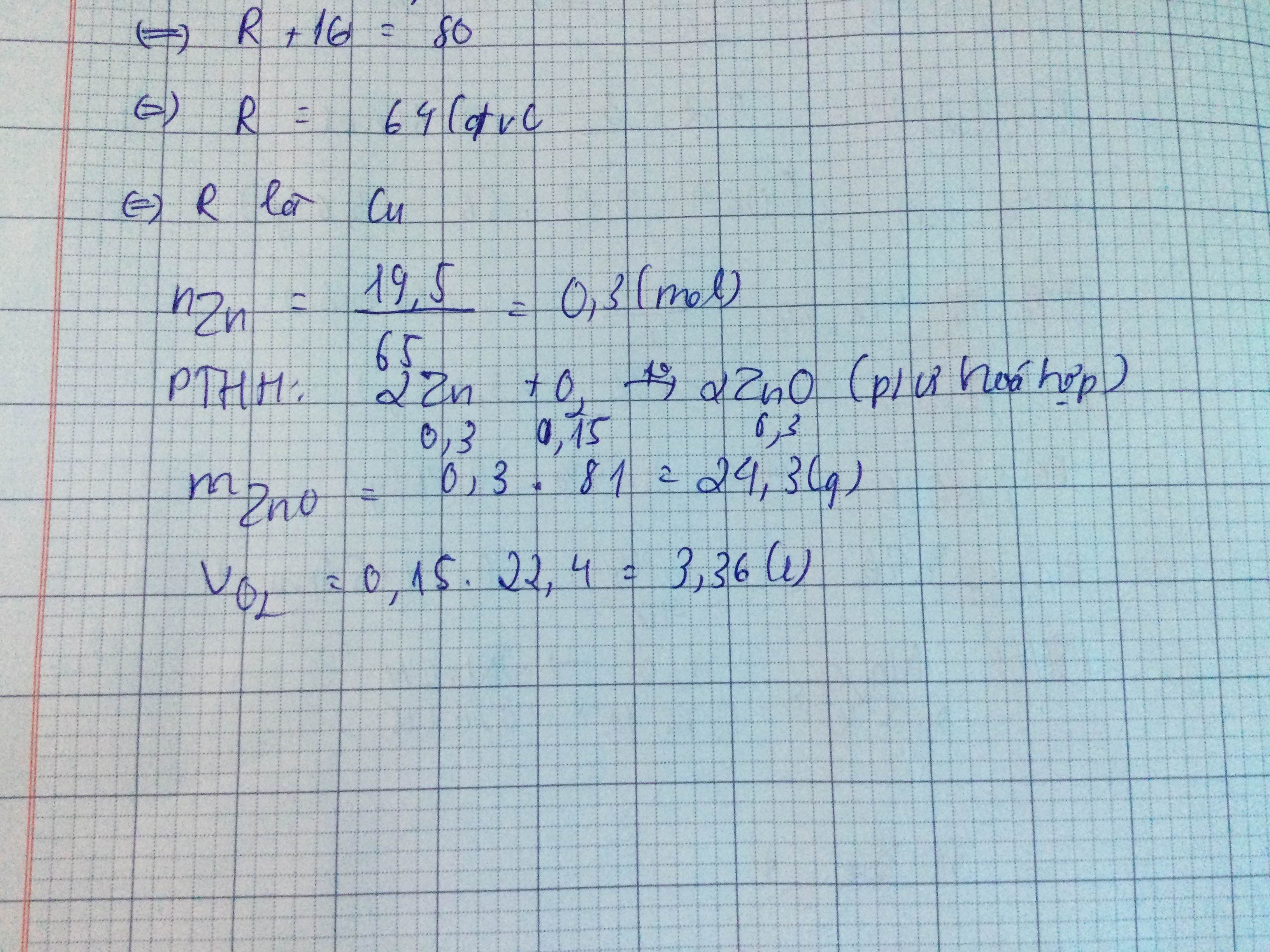
\(n_{Fe}=\dfrac{126}{56}=2,25\left(mol\right)\\ PTHH:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\\ Mol:2,25\rightarrow1,5\left(mol\right)\\ PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ Mol:1\leftarrow1\leftarrow1,5\\ m_{KClO_3}=1.122,5=122,5\left(g\right)\)
giúp mình với