Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Có 2R+(96x3)=342
Suy ra: R=27 là nhôm(Al)
b) MB=32x0,5=16
Suy ra: MA=16x2,125=34
Ta có : HuSv
5,88%=100u/34 =>u=2
94,12%=32 x 100 x v/34 => v=1
Vậy công thức hoá học của A là: H2S
Chúc bạn học tốt!

Đ
ặ
t
:
Y
(
N
O
3
)
2
V
ì
:
%
m
Y
=
34
,
043
%
⇔
M
Y
M
Y
+
124
=
34
,
043
%
⇔
M
Y
=
64
(
g
m
o
l
)
⇒
Y
:
Đ
ồ
n
g
(
C
u
=
64
)
⇒
C
T
H
H
:
C
u
(
N
O
3
)
2
Thu gọn

1. Gọi CTHH của oxit là NxOy.
Ta có: \(\dfrac{m_N}{m_O}=\dfrac{7}{20}\Rightarrow\dfrac{n_N}{n_O}=\dfrac{7}{20}:\dfrac{14}{16}=\dfrac{2}{5}\)
⇒ x:y = 2:5
→ N2O5
2. Gọi CTHH cần tìm là FexOy.
\(\Rightarrow\dfrac{m_{Fe}}{m_O}=\dfrac{7}{2}\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{7}{2}:\dfrac{56}{16}=1\)
⇒ x:y = 1
→ FeO
3. CTHH cần tìm: RO2
Mà: %R = 46,7%
\(\Rightarrow\dfrac{M_R}{M_R+16.2}.100\%=46,7\%\)
⇒ MR = 28 (g/mol)
→ SiO2


Tham khảo nhé :
Nguồn: Phần trăm khối lượng của nguyên tố R trong hợp chất khí với hidro | VietJack.com

b,
Ta có: dX/O2=1,375
=>Mx =1,375.32
=44(g/mol)
Ta lại có:
12.x/27,27=16.y/72,73=44/100
=>x=27,27.44/12.100=1
=> y=72,73.44/16.100=2
Vậy CTHH: CO2

\(a,M_A=1,8125.32=58(g/mol)\)
Trong 1 mol A: \(\begin{cases} n_C=\dfrac{58.82,75\%}{12}=4(mol)\\ n_H=\dfrac{58-4.12}{1}=10(mol) \end{cases}\)
\(\Rightarrow CTHH_A:C_4H_{10}\\ b,n_C=\dfrac{2,88}{12}=0,24(mol)\\ \Rightarrow n_A=\dfrac{1}{4}n_C=0,06(mol)\\ \Rightarrow m_A=0,06.58=3,48(g)\\ c,n_A=\dfrac{11,6}{58}=0,2(mol)\\ \Rightarrow \begin{cases} n_C=0,2.4=0,8(mol)\\ n_H=0,2.10=2(mol) \end{cases}\Rightarrow \begin{cases} m_C=0,8.12=9,6(g)\\ m_H=2.1=2(g) \end{cases}\)

Công thức của oxit là A l x O y
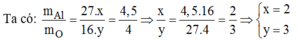
Vậy công thức hóa học của nhôm oxit là A l 2 O 3 .

Hợp chất khí của R với hidro là RH2
=> hóa trị cao nhất của R khi kết hợp với oxi là : 8-2=6, vậy ct hợp chất của R và oxi là RO3
tỉ lệ khối lượng giữa R và oxi: MR/MO =2/3
=> 3R= 16.3.2 =>R=32. Vậy R là lưu huỳnh
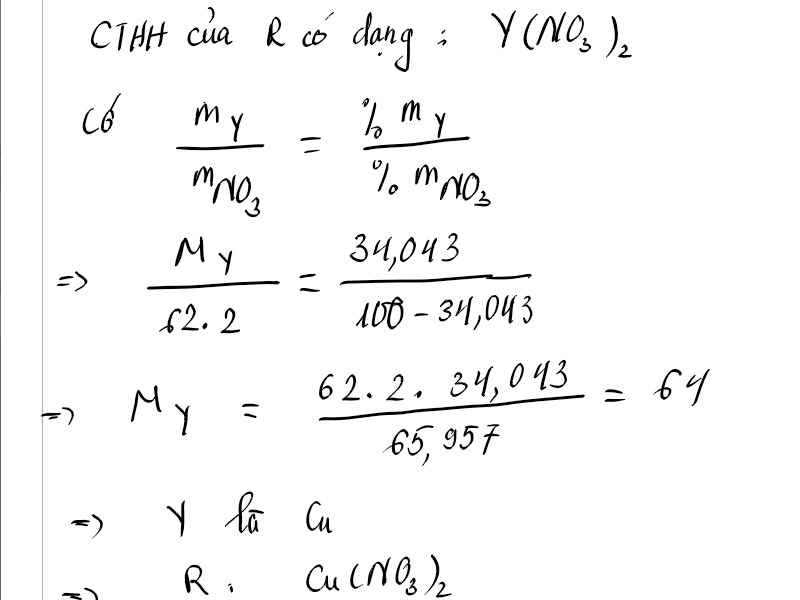
Gọi công thức của A và B lần lượt là R2Oa và R2Ob (a<b, a và b chẵn).
Ta có: \(\dfrac{16a}{2M_R+16a}=57,14\%\) \(\Rightarrow\) MR=\(\dfrac{17144}{2857}\)a.
dB/A=\(\dfrac{M_B}{M_A}=\dfrac{2M_R+16b}{2M_R+16a}=\dfrac{\dfrac{34288}{2857}a+16b}{\dfrac{80000}{2857}a}=1,5714\) \(\Rightarrow\) 2a=b.
Chỉ có a=2, b=4 thỏa mãn: MR\(\approx\)12 (g/mol), R là cacbon, A và B là CO và CO2.