Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy NaX và NaY về NaR
\(n_{AgNO_3}=0,15.0,2=0,05\left(mol\right)\)
PTHH: \(AgNO_3+NaR\rightarrow AgR\downarrow+NaNO_3\)
0,05------>0,05
\(\rightarrow M_R=\dfrac{2,2}{0,05}=44\left(g\text{/}mol\right)\)
Mà X và Y là 2 nguyên tố halogen thuộc 2 chu kì liên tiếp
\(\rightarrow M_X< M_R< M_Y\rightarrow M_X< 44< M_Y\)
---> X và Y là Cl và Br

- Nếu chỉ một trong hai muối tác dụng với Bạc nitrat :
Suy ra hai muối là NaCl và NaF
\(AgNO_3 + NaCl \to AgCl + NaNO_3\\ n_{NaCl} = n_{AgCl} = \dfrac{43,2}{143,5} = 0,3(mol)\\ \Rightarrow m_{NaCl} = 0,3.58,5 = 17,55 < 25,3(\text{thỏa mãn})\)
- Nếu cả hai muối đều tác dụng với Bạc nitrat :
Gọi CTTQ của hai muối : NaX
\(NaX + AgNO_3 \to AgX + NaNO_3\\ n_{NaX} = n_{AgX} \\ \Leftrightarrow \dfrac{25,3}{23 + X} = \dfrac{43,2}{108+X}\\ \Rightarrow X = 97,13\\ M_{Br} = 80 < M_X = 97,13 < M_I = 127\)
Vậy hai muối là NaBr và NaI

+) Trường hợp 1: Hỗn hợp gồm NaF và NaCl
PTHH: \(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Ta có: \(n_{AgCl}=\dfrac{2,87}{143,5}=0,02\left(mol\right)=n_{NaCl}\)
\(\Rightarrow m_{NaCl}=0,02\cdot58,5=1,17\left(g\right)\) \(\Rightarrow m_{NaF}=0,415\left(g\right)\)
+) Trường hợp 2: Hỗn hợp không chứa NaF
Gọi công thức chung 2 muối là NaR
PTHH: \(NaR+AgNO_3\rightarrow NaNO_3+AgR\downarrow\)
Theo PTHH: \(n_{NaR}=n_{AgR}\) \(\Rightarrow\dfrac{1,595}{23+\overline{M}_R}=\dfrac{2,87}{108+\overline{M}_R}\)
\(\Rightarrow\overline{M}_R\approx83,3\) \(\Rightarrow\) 2 halogen cần tìm là Brom và Iot
Vậy 2 muối có thể là (NaF và NaCl) hoặc (NaBr và NaI)
*P/s: Các phần còn lại bạn tự làm

Đáp án D
Trường hợp 1: Hai halogen đều tạo được kết tủa với AgNO3
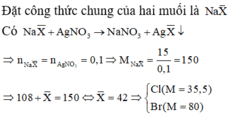
Do đó hai muối trong X là NaCl và NaBr
Trường hợp 2: Hai muối là NaF và NaCl
Phản ứng tạo thành kết tủa chỉ có AgCl và AgF là muối tan:
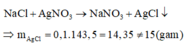
Do đó trường hợp này không thỏa mãn.

a)
Gọi CTHH của hai muối là NaR
\(NaR +AgNO_3 \to AgR + NaNO_3\)
Ta có:
\(n_{NaR} = n_{AgNO_3} = 0,2.0,1 = 0,02(mol)\\ \Rightarrow 23 + R = \dfrac{1,615}{0,02} = 80,75\\ \Rightarrow R = 57,75\)
Vì MCl = 35,5 < R = 57,75 <MBr = 80 nên 2 muối là NaCl và NaBr
b)
\(\left\{{}\begin{matrix}NaCl:x\left(mol\right)\\NaBr:y\left(mol\right)\end{matrix}\right.\)→ \(\left\{{}\begin{matrix}58,5x+103y=1,615\\x+y=0,02\end{matrix}\right.\)→\(\left\{{}\begin{matrix}x=0,01\\y=0,01\end{matrix}\right.\)
Vậy :
\(\%m_{NaCl} = \dfrac{0,01.58,5}{1,615}.100\% = 36,22\%\\ \%m_{NaBr} = 100\% - 36,22\% = 63,78\%\)
c)
\(\left\{{}\begin{matrix}AgCl:x=0,01\left(mol\right)\\AgBr:y=0,01\left(mol\right)\end{matrix}\right.\)→ mkết tủa = 0,01.143,5 + 0,01.188=3,315(gam)
\(n_{AgNO_3}=0.2\cdot0.1=0.02\left(mol\right)\)
\(TH1:X:F\\ Y:Cl\)
\(NaCl+AgNO_3\rightarrow NâNO_3+AgCl\)
\(0.02........0.02............0.02..........0.02\)
\(m_{NaCl}=0.02\cdot58.5=1.17\left(g\right)< 1.615\left(g\right)\)
\(\%NaCl=\dfrac{1.17}{1.615}\cdot100\%=72.45\%\)
\(\%NaF=100-72.45=27.55\%\)
\(m_{AgCl}=0.02\cdot143.5=2.87\left(g\right)\)
\(TH2:Đặt:NaZ\)
\(NaZ+AgNO_3\rightarrow NaNO_3+AgZ\)
\(0.02.........0.02\)
\(M_{NaZ}=\dfrac{1.615}{0.02}=80.75\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow23+Z=80.75\\ \Rightarrow Z=57.75\)
\(X< Z< Y\Rightarrow X:Cl,Y:Br\)
\(Đặt:n_{NaCl}=a\left(mol\right),n_{NaBr}=b\left(mol\right)\)
\(\left\{{}\begin{matrix}a+b=0.02\\58.5a+103b=1.615\end{matrix}\right.\)
\(\Rightarrow a=b=0.01\)
\(\%NaCl=\dfrac{0.01\cdot58.5}{1.615}\cdot100\%=36.22\%\)
\(\%Nà=100-36.22=63.78\%\)
\(m_{\downarrow}=m_{AgCl}+m_{AgBr}=0.01\cdot143.5+0.01\cdot188=3.315\left(g\right)\)




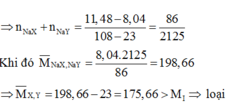

\(NaR+AgNO_3\rightarrow AgR+NaNO_3\)
0,03_____0,03_____________________
\(n_{AgNO3}=0,15.0,2=0,03\left(mol\right)\)
\(M_{NaR}=\frac{2,2}{0,03}=73,333\)
\(\rightarrow R=50,333\)
\(Cl< R< Br\)