Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

VCO2=65-25=40cm3
BT O : VH2O= 2*(80-65) = 30cm3
----> C : H = 40 : 60
-----> C4H6

\(20cm^3\) khí thoát ra là \(O_2\)
\(\Rightarrow V_{O_2\left(d\text{ư}\right)}=20\left(cm^3\right)\Rightarrow\left\{{}\begin{matrix}V_{O_2\left(p\text{ư}\right)}=70-20=50\left(cm^3\right)\\V_{CO_2}+V_{H_2O}=90-20=70\left(cm^3\right)\end{matrix}\right.\)
Đặt CTPT của hiđrocacbon là \(C_xH_y\left(x,y\in N\text{*}\right)\)
Vì các khí đo ở cùng điều kiện nên tỉ lệ thể tích cũng là tỉ lệ mol
\(\Rightarrow n_{C_xH_y}:n_{O_2}:\left(n_{CO_2}+n_{H_2O}\right)=V_{C_xH_y}:V_{O_2}:\left(V_{CO_2}+V_{H_2O}\right)=10:50:70=1:5:7\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}+n_{H_2O}=7n_{C_xH_y}\\n_{O_2}=5n_{C_xH_y}\end{matrix}\right.\)
PTHH: \(C_xH_y+\left(x+\dfrac{y}{4}\right)O_2\xrightarrow[]{t^o}xCO_2+\dfrac{y}{2}H_2O\)
\(\Rightarrow\left\{{}\begin{matrix}x+\dfrac{y}{2}=7\\x+\dfrac{y}{4}=5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=3\\y=8\end{matrix}\right.\left(TM\right)\)
Vậy CTPT của hiđrocacbon là \(C_3H_8\)

Đáp án A
Theo giả thiết, ta có :
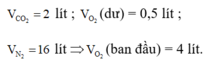
Sơ đồ phản ứng :
CxHy + O2 → CO2 +H2O + O2 dư
lít: 1 4 2 a 0,5
Áp dụng định luật bảo toàn nguyên tố đối với các nguyên tố C, H, O ta có :
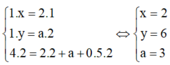
Þ Công thức của hiđrocacbon là C2H6

Xem tỉ lệ thể tích tương ứng tỉ lệ số mol
\(n_{O_2\left(pư\right)}=80-25=55\left(mol\right)\)
\(n_{CO_2}=65-25=40\left(mol\right)\)
\(BTNTO:2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=2\cdot55-2\cdot40=30\left(mol\right)\)
\(Đặt:CTHH:C_xH_y\)
\(x=\dfrac{n_{CO_2}}{n_X}=\dfrac{40}{10}=4\)
\(y=\dfrac{2n_{H_2O}}{n_X}=\dfrac{60}{10}=6\)
\(CTPT:C_4H_6\)