Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 2
Gọi x, y là số mol củaCuO và ZnOmol HCl=3.0,1=0,3mol(100ml=0,1l)
CuO+2HCl->CuCl2+H2O (1)
xmol 2xmol
ZnO+2HCl->ZnCl2+H2O(2)
ymol 2ymol
Từ 1 và 2 ta co hệ phương trình
2x+2y=0,3 ->x=0,05=molCuO
80x+81y=12,1 ->y=0,1=molZnO
=>mCuO=0,05.80=4g
->%CuO=(4.100)/12,1=33,075%
->%ZnO=100-33,075=66,943%
b. CuO+H2SO4->CuSO4+H2O (3)
Theo ptpu 3 taco nH2SO4=nCuO=0,05 mol
ZnO+H2SO4->ZnSO4+H2O (4)
Theo ptpu 4 ta co nH2SO4=nZnO=0,1mol
=>nH2SO4=0.05+0,1=0,15mol
->mH2SO4=0,15.98=14,7g
=>mddH2SO4=(14,7.100)/20=73,5g
Bài 1
a/. Phương trình phản ứng hoá học:
Fe + 2HCl --> FeCl2 + H2
b/. nH2 = V/22,4 = 3,36/22,4 = 0,15 (mol)
....... Fe.....+ 2HCl --> Fecl2 + H2
TPT 1 mol....2 mol.................1 mol
TDB x mol....y mol................0,15 mol
nFe = x = (0,15x1)/1 = 0,15 (mol)
mFe = n x M = 0,15 x 56 = 8,4 (g)
c/. nHCl = y = (0,15x2)/1 = 0,3 (mol)
CMHCl = n/V = 0,3/0,05 = 6 (M)

a)
$Fe + 2HCl \to FeCl_2 + H_2$
b) Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
c) $n_{HCl} = 2n_{H_2} = 0,3(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,3}{0,05} = 6M$
d) $2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{H_2SO_4} = \dfrac{1}{2}n_{NaOH} = 0,25(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,25.98}{20\%} = 122,5(gam)$
$V_{dd\ H_2SO_4} = \dfrac{122,5}{1,14} = 107,5(ml)$

a)
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$ZnO + H_2SO_4 \to ZnSO_4 +H_2O$
b) Gọi $n_{CuO} = a(mol) ; n_{ZnO} = b(mol) \Rightarrow 80a +81b = 12,1(1)$
Theo PTHH :
$n_{H_2SO_4} = a + b = \dfrac{73,5.20\%}{98} = 0,15(mol)(2)$
Từ (1)(2) suy ra : a = 0,05 ; b = 0,1
$\%m_{CuO} = \dfrac{0,05.80}{12,1}.100\% = 33,06\%$
$\%m_{ZnO} = 100\% - 33,06\% = 66,94\%$

\(n_{FeO}=a\left(mol\right),n_{CuO}=b\left(mol\right)\)
\(m_{hh}=72a+80b=19.2\left(g\right)\left(1\right)\)
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(n_{H_2SO_4}=a+b=0.25\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.15\)
\(m_{FeO}=0.1\cdot72=7.2\left(g\right)\)
\(m_{CuO}=12\left(g\right)\)
\(C_{M_{FeSO_4}}=\dfrac{0.1}{0.25}=0.4\left(M\right)\)
\(C_{M_{CuSO_4}}=\dfrac{0.15}{0.25}=0.6\left(M\right)\)

200 ml =0,2 l
nHCl=0,2.3=0,6(mol)
CuO+2HCl−>CuCl2+H2O(1)
a 2a (mol)
ZnO+2HCl−>ZnCl2+H2O(2)
b 2b (mol)
ta có
{80a+81b=24,2
2a+2b=0,6{
giả ra ta được a =0,1 (mol)
=> mCuO=0,1.80=8(g)
thành phần % theo khối lượng mỗi oxit trong hỗn hợp ban đầu là
%CuO = 824,2.100%=33,06%
%ZnO= 100% - 33,06% = 66,94%

Đổi 300ml = 0,3 lít
Ta có: \(n_{HCl}=2.0,3=0,6\left(mol\right)\)
a. PTHH:
CuO + 2HCl ---> CuCl2 + H2O (1)
ZnO + 2HCl ---> ZnCl2 + H2O (2)
b. Gọi x, y lần lượt là số mol của CuO và ZnO
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{ZnO}=2y\left(mol\right)\)
=> 2x + 2y = 0,6 (*)
Theo đề, ta có: 80x + 81y = 24,2 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+2y=0,6\\80x+81y=24,2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(m_{CuO}=0,1.80=8\left(g\right)\)
=> \(\%_{m_{CuO}}=\dfrac{8}{24,2}.100\%=33,06\%\)
\(\%_{m_{Zn}}=100\%-33,06\%=66,94\%\)
c. PTHH:
CuO + H2SO4 ---> CuSO4 + H2O (3)
ZnO + H2SO4 ---> ZnSO4 + H2O (4)
Theo PT(3): \(n_{H_2SO_4}=n_{CuO}=0,1\left(mol\right)\)
Theo PT(4): \(n_{H_2SO_4}=n_{ZnO}=0,2\left(mol\right)\)
=> \(n_{H_2SO_4}=0,1+0,2=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{29,4}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)

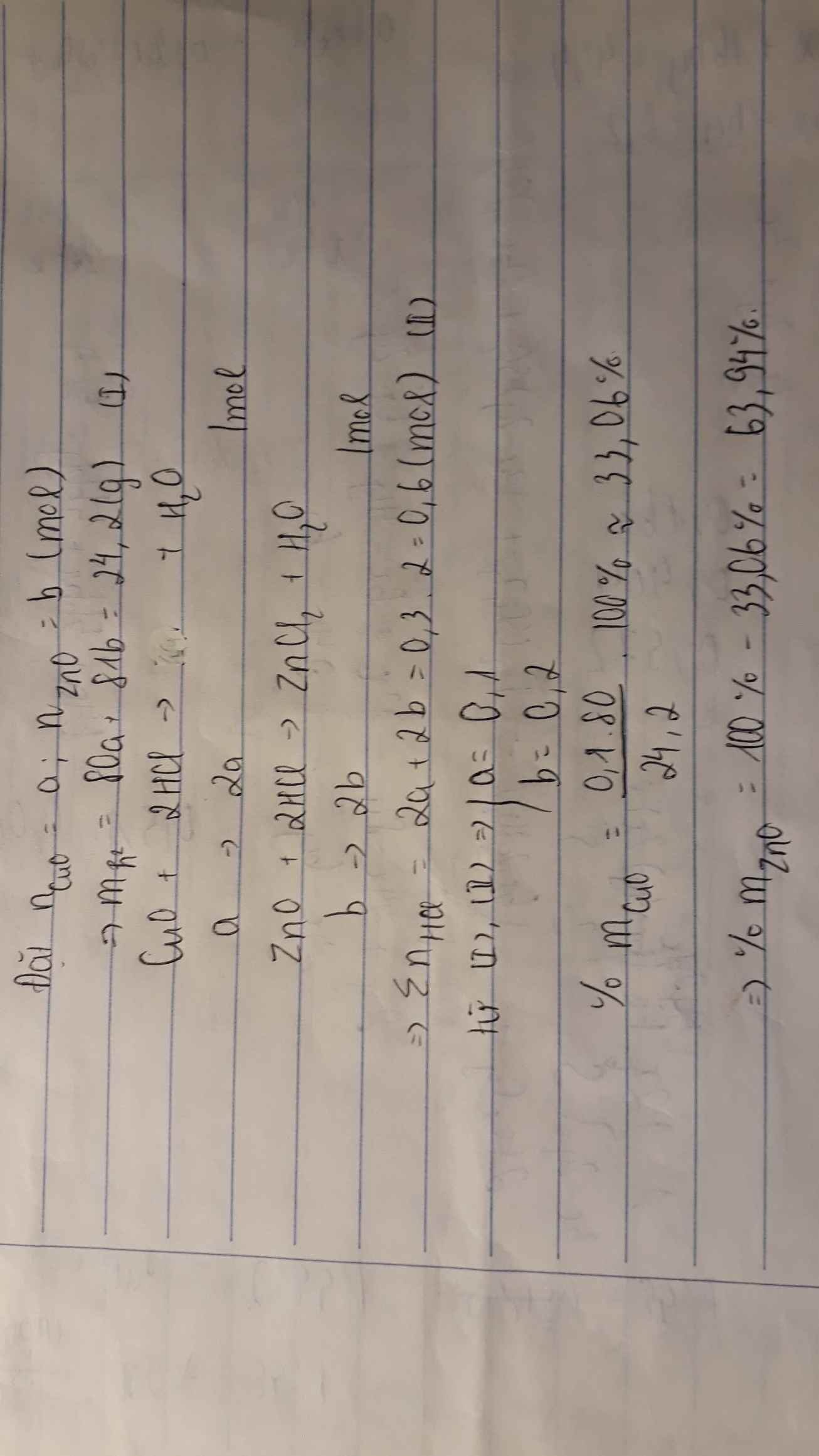
Bài 2 :
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Bài 3 :
a) Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
a 2a
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O|\)
1 2 1 1
b 2b
b) Gọi a là số mol của CuO
b là số mol của ZnO
\(m_{CuO}+m_{ZnO}=12,1\left(g\right)\)
⇒ \(n_{CuO}.M_{CuO}+n_{ZnO}.M_{ZnO}=12,1g\)
⇒ 80a + 81b = 12,1g (1)
Ta có : 100ml = 0,1l
\(n_{HCl}=3.0,1=0,3\left(mol\right)\)
⇒ 2a + 2b = 0,3(2)
Từ (1),(2), ta có hệ phương trình :
80a + 81b = 12,1g
2a + 2b = 0,3
⇒ \(\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
\(m_{CuO}=0,05.80=4\left(g\right)\)
\(m_{ZnO}=0,1.81=8,1\left(g\right)\)
0/0CuO = \(\dfrac{4.100}{12,1}=33,06\)0/0
0/0ZnO = \(\dfrac{8,1.100}{12,1}=66,94\)0/0
c) Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,05 0,05
\(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O|\)
1 1 1 1
0,1 0,1
\(n_{H2SO4\left(tổng\right)}=0,05+0,1=0,15\left(mol\right)\)
\(m_{H2SO4}=0,15.98=14,7\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{14,7.100}{20}=73,5\left(g\right)\)
Chúc bạn học tốt