Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các câu lý thuyêt này mình tưởng em tra trong sách đang học là có hết rồi chứ nhỉ?

Câu 1: B
Cấu hình: 1s22s22p63s23p4
=> Z = 16
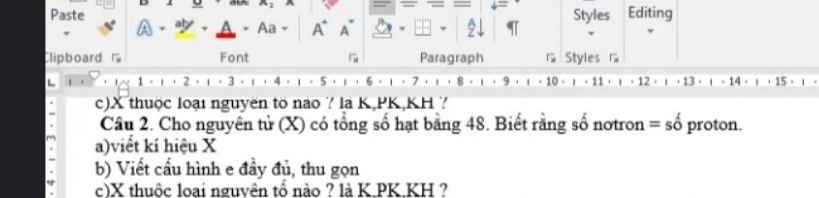
Câu 2: A
X có lớp e ngoài cùng thuộc lớp N => Có 4 lớp e
Cấu hình: 1s22s22p63s23p63d34s2
Câu 3: B
Số e = Z = 19
Câu 1: B
Cấu hình: 1s22s22p63s23p4
=> Z = 16
Câu 2: A
X có lớp e ngoài cùng thuộc lớp N => Có 4 lớp e
Cấu hình: 1s22s22p63s23p63d34s2
Câu 3: B
Số e = Z = 19

Al : 1s22s22p63s23p1 ( kim loại vì lớp e ngoài cùng có 3e)
S : 1s22s22p63s23p4 ( phi kim vì lớp e ngoài cùng có 6e )
O : 1s22s22p4 ( phi kim vì lớp e ngoài cùng có 6e )
Fe : 1s22s22p63s23p63d64s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cu : 1s22s22p63s23p63d104s1 ( kim loại vì lớp e ngoài cùng có 1e )
Zn : 1s22s22p63s23p63d104s2 ( kim loại vì lớp e ngoài cùng có 2e )
Cl : 1s22s22p63s23p5 ( kim loại vì lớp e ngoài cùng có 7e )
K : 1s22s22p63s23p64s1 ( kim loại vì lớp e ngoài cùng có 1e )
Br : 1s22s22p63s23p63d104s24p5 (kim loại vì lớp e ngoài cùng có 7e )
Ne : 1s22s22p6 ( khí hiếm vì lớp e ngoài cùng có 8e )
- Nguyên tố s : K ( e cuối cùng điền vào phân lớp s )
- Nguyên tố p : O, Ne, S, Cl, Br, Al ( e cuối cùng điền vào phân lớp p )
- Nguyên tố d : Fe, Cu, Zn ( e cuối cùng điền vào phân lớp d )
13.
Hoá trị 1 nguyên tố trong hợp chất: số liên kết nguyên tử nguyên tố đó tạo thành trong hợp chất đó.
Có thể dựa vào số e hoá trị của 1 nguyên tố để xác định hoá trị:
- Be: Hoá trị trong hợp chất là II.
- C: trạng thái cơ bản hoá trị II. Sau khi kích thích lên 4e độc thân thì hoá trị IV.
- S: trạng thái cơ bản hoá trị II. Sau khi kích thích lên 4e độc thân thì hoá trị IV. Kíc thích tiếp lên 6e độc thân thì hoá trị VI.
14.
- Lai hoá là sự trộn lẫn các obitan cơ bản để tạo các obitan lai hoá tham gia liên kết.
- Các kiểu lai hoá thường gặp: \(sp^3,sp^2,sp\)
- Ý nghĩa: giải thích trật tự liên kết một số hợp chất không nghiệm đúng với bát tử (PCl5), giải thích góc hình học các liên kết.
- Đặc điểm obitan lai hoá: năng lượng bằng nhau và sắp xếp trong không gian sao cho năng lượng là nhỏ nhất.
15.
- BeH2: Be kích thích lên 2e độc thân. Hai obitan mang e độc thân lai hoá sp. Hai obitan lai hoá xen phủ trục với 2 H để tạo liên kết.
- CH4: C kích thích lên 4e độc thân. Bốn obitan mang e độc thân lai hoá sp3. Bốn obitan lai hoá xen phủ trục với 4 H để tạo liên kết.
- C2H5OH: Mỗi C kích thích lên 4e độc thân, sau đó lai hoá sp3. Ba obitan C thứ nhất xen phủ 3 obitan lai hoá với 3 H, obitan còn lại xen phủ với C thứ hai. Hai obitan C thứ hai xen phủ tiếp với 2 H, obitan còn lại xen phủ với obitan của O trong nhóm OH.
- C2H4: Mỗi C kích thích lên 4e độc thân. Hai C tiến hành lai hoá sp2. Với mỗi C, 2 obitan lai hoá xen phủ với 2 H, obitan lai hoá thứ ba xen phủ với C còn lại. Mỗi obitan cơ bản mang e độc thân của mỗi C xen phủ bên với nhau tạo liên kết ππ.
- C2H2: Mỗi C kích thích lên 4e độc thân. 2 C tiến hành lai hoá sp. Với mỗi C, 1 obitan lai hoá xen phủ với 1 H, obitan lai hoá kia xen phủ với C còn lại. Hai obitan cơ bản mang e độc thân của mỗi C xen phủ bên tạo 2 liên kết ππ.
- CO2: C kích thích lên 4e độc thân. C tiến hành lai hoá sp. Hai obitan lai hoá liên kết với 2 O xung quanh. Do mỗi O còn dư 1e độc thân nên tạo liên kết ππ với obitan cơ bản mang e độc thân của C.
- SO2: S kích thích lên 4e độc thân. S tiến hành lai hoá sp2. Một obitan lai hoá dành cho cặp e ghép đôi chưa liên kết. Hai obitan lai hoá còn lại tạo liên kết với O.
- SO3: S kích thích lên 6e độc thân. S tiến hành lai hoá sp2. Mỗi obitan đều xen phur với 1 O tạo liên kết.
- CH3Cl: C kích thích lên 4e độc thân, lai hoá sp3. Mỗi obtan lai hoá xen phủ với 1 phối tử.
- NH3: N lai hoá sp3. Một obitan lai hoá dành cho cặp e chưa liên kết. Ba obitan còn lại xen phủ với 3 H.
- H2O: O lai hoá sp3. Hai obitan lai hoá dành cho 2 cặp e chưa liên kết, 2 obitan còn lại liên kết với 2 H.
- NF3: N lai hoá sp3. Một obitan dành cho cặp e chưa liên kết, còn lại xen phủ với 3 H.