Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đầu tiên là F fluorine số electon 19 stt 9 chu kì 2 nhóm VIIA
Thứ 2 là sodium số electon 23 stt 11 chu kì 3 nhóm IA
Cuối cùng là scandium số electon là 45 stt 21 chu kì 4 nhóm IIIB

- Xét nguyên tố có số thứ tự 9:
+ Nằm ở nhóm VIIA => Có 7 electron ở lớp vỏ ngoài cùng và thuộc phi kim hoạt động mạnh
- Xét nguyên tố có số thứ tự 18:
+ Nằm ở nhóm VIIIA => Có 8 electron ở lớp vỏ ngoài cùng và là khí hiếm
- Xét nguyên tố có số thứ tự 19:
+ Nằm ở nhóm IA => Có 1 electron ở lớp vỏ ngoài cùng thuộc kim loại hoạt động mạnh

Cấu hình: 1s22s22p63s23p3
=> Vì e ngoài cùng điền ở phân lớp 3p, và có 5e lớp ngoài cùng
=> Nguyên tử nguyên tố này thuộc chu kì 3 và có 3 lớp e

`1,`
Số electron lớp ngoài cùng của nguyên tử nguyên tố `Al` là `3`
Gt: Nguyên tố `Al` thuộc nhóm `IIIA`
Vì số nhóm `A` bằng số electron lớp ngoài cùng của các nguyên tử nguyên tố thuộc nhóm đó `-> Al` có `3e` lớp ngoài cùng.
Tương tự, `Cl` thuộc nhóm `VIIA ->` nguyên tố `Cl` có `7e` lớp ngoài cùng.
`2,`
Các nguyên tố thuộc chu kì và cùng nhóm với nguyên tố `Be:`
Chu kì: `Li, B, C, N, O, F, Ne`
Nhóm: `Mg, Ca, Sr, Ba, Ra`
1. Cấu hình e của Al (Z=13): 1s22s22p63s23p1
=> Có 3e lớp ngoài cùng (3e lớp thứ 3)
Cấu hình e của S (Z=16): 1s22s22p63s23p23p4
=> Có 6e lớp ngoài cùng (6e lớp thứ 3)

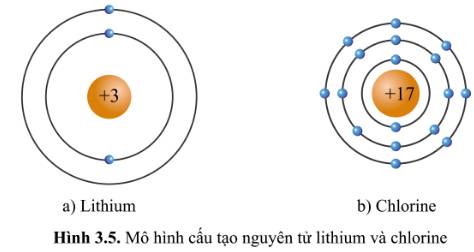
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA

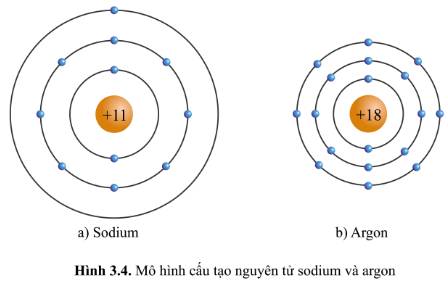
- Xét mô hình nguyên tử natri:
+ Số hiệu nguyên tử: 11
+ Điện tích hạt nhân: +11
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp ngoài cùng
- Xét mô hình nguyên tử argon:
+ Số hiệu nguyên tử: 18
+ Điện tích hạt nhân: +18
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 8 hình tròn xanh ở vòng tròn ngoài cùng => Có 8 electron ở lớp ngoài cùng

a)
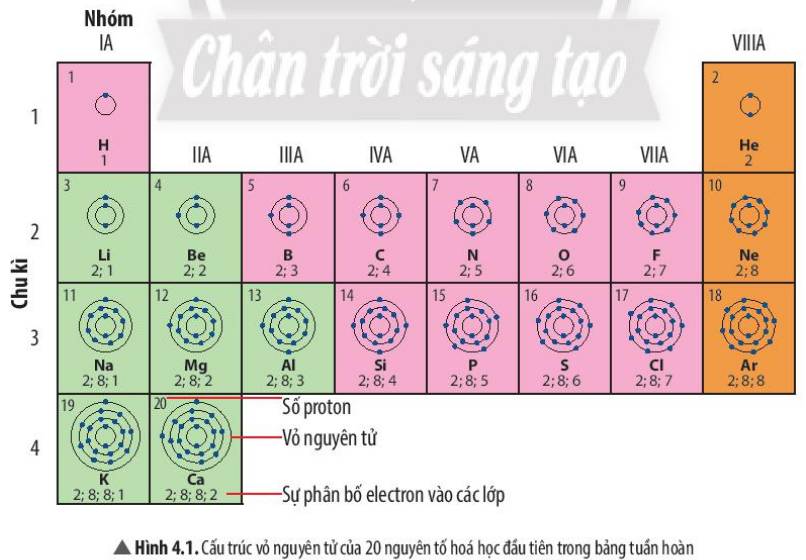
1 lớp:H,He
2 lớp:Li, Be, B, C, N, O, F
3 lớp:Na, Mg, Al, Si, P, S, Cl, Ar
4 lớp:K,Ca
b)
1 e ngoài cùng:H, Li, Na, K
2 e ngoài cùng:Be, Mg, Ca
3 e ngoài cùng:B, Al

- Nguyên tố carbon:
+ Có số hiệu nguyên tử: 6
+ Nằm ở chu kì 2 => Có 2 lớp electron
- Nguyên tố nhôm:
+ Có số hiệu nguyên tử: 13
+ Nằm ở chu kì 3 => Có 3 lớp electron

- Nguyên tố X nằm ở chu kì 2, nhóm VA => Hàng số 2, cột VA
=> Nguyên tố phosphorus
+ Tên nguyên tố: Phosphorus
+ Kí hiệu hóa học: P
+ Khối lượng nguyên tử: 31
+ Ví trí ô của nguyên tố trong bảng tuần hoàn = số hiệu nguyên tử = 15
+ Ô nguyên tố có màu hồng => Phi kim
Nguyên tố X nằm ở chu kì 3, thuộc nhóm VIA
ơ kìa:< Sao cậu lại chiếm box tự nhiên của tớ, về box anh chơi đi chứ:)))).