Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
X và Y đều phản ứng với AgNO3/NH3 tạo nAg = 4nX(Y)
=> X là : OHC – CO – CHO
Y là : OHC – CH2 – CHO ; HCOOCH=CH2

Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp s là 7=> các e đó nằm ở
1s,2s,3s,4s.
X có 6 e độc thân => [Ar] 3d54s1 => X là Cr
=> Y có số hạt mang điện là 16 => số p là 8 => Y là O
=> hợp chất của X và Y lưỡng tính => đó phải là Cr2O3
=> C

Chọn A.
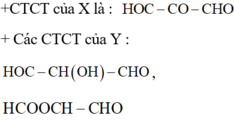
+ CTCT của X là: HOC - CO - CHO.
+ Các CTCT của Y: HOC - CH(OH) - CHO, HCOOCH - CHO.

Chọn C.
Dựa vào tỉ lệ khối lượng ta thấy 1 mol X tác dụng tối đa 2 mol NaOH
Các công thức cấu tạo của X thoả mãn là HCOOC6H4CH3 (o, m, p) và CH3COOC6H5.

Chọn A.
Trong 1 mol hơi chất Y có 122 (C7H6O2)
+ Các đồng phân của X là HOC6H4CHO (o, m, p)
+ Các đồng phân của Y là C6H5COOH
Vậy tổng đồng phân của X và Y là 4

Đáp án C
Thí nghiệm xảy ra ăn mòn điện hóa là (2), (5) và (7) + Loại (3) vì Cu và Ag đều không tác dụng với HCl.
+ Loại (4) vì thiếc (Sn) tráng thanh sắt (Fe)
⇒ Không có 2 kim loại nhúng trong cùng 1 dung dịch chất điện li.
+ Loại (6) vì không thỏa điều kiện nhúng trong dung dịch chất điện ly

HD:
Gọi Z,N tương ứng là số hạt proton và notron của X; Z', N' là số hạt proton và notron của Y.
Số khối của X là A = Z + N = 2Z (vì N = Z đề bài cho); số khối của Y là A' = Z' + N' = 2Z'.
Trong XY2, X chiếm 50% khối lượng nên: 2Z/(2Z + 4Z') = 0,5 hay Z = 2Z' (1).
Tổng số proton trong XY2 là 32 nên: Z + 2Z' = 32 (2) kết hợp với (1) ta có: Z = 16 (S) và Z' = 8 (O).
a) X: 1s22s22p63s23p4; Y: 1s22s22p4
b) Công thức phân tử: SO2; cấu tạo: O = S = O