Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Công thức hóa học của hợp chất là A l 2 O 3
Phân tử khối: 27.2 + 16.3 = 102 đvC.

Gọi CTHH là Z2O5
% O = 16.5 / ( MZ.2+16.5)= 56,34%
<=> MZ ∼ 31 đvc
=> Z là photpho (P)
=> CTHH là P2O5
M P2O5 = 31.2+16.5=142 đvc

Gọi công thức của hợp chất là T 2 O 3 và a là nguyên tử khối của T.
Theo đề bài, ta có tỉ lệ phần trăm khối lượng của T:
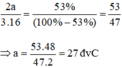
Nguyên tố T là nhôm.

Gọi CTHH của hợp chất là TxOy
Theo quy tắc hóa trị ta có :
III.x=II.y \(\Rightarrow\frac{x}{y}=\frac{II}{III}=\frac{2}{3}\)
Vậy CTHH của hợp chất là T2O3
Ta có : T chiếm 53% nên O chiếm 47%
Ta lại có:
\(x:y=\frac{\text{%T}}{M_T}:\frac{\%O}{M_O}=\frac{53}{M_T}:\frac{47}{16}\)
\(\Leftrightarrow\frac{2}{3}=\frac{53}{M_T}:\frac{47}{16}=\frac{53}{M_T}.\frac{16}{47}\)
\(\Rightarrow M_T=\frac{3.53.16}{2.47}\approx27\)
Vậy T là nhôm. KHHH : Al
\(\Rightarrow\) CTHH của hợp chất là Al2O3
Phân tử khối của Al2O3 = 27.2+16.3 = 102(đvC)

Gọi CTTQ: AxOy
Hóa trị của A: 2y/x
\(\frac{70}{30}=\frac{x.M_{A}}{y.16}\)
<=>\(\frac{56}{3}.\frac{2y}{x}=\frac{16y.7}{3x}=\frac{16y.70}{30x}= M_{A}\)
Biện luận:
| 2y/x | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| MA | 18,67 (loại) | 37,3 (loại) | 56 (nhận) | 74,68 (loại) | 93,35 (loại) | 112,02 (loại) | 130,69 (loại) |
Vậy A là Sắt (Fe)
CTHH: Fe2O3

Gọi công thức tổng quát là $XH_4$
\(\%H=25\%\\ \Rightarrow \dfrac{4}{X+4}.100\%=25\%\\ \Rightarrow X=12\\ Tên:\ Cacbon\\ CTHH:\ CH_4\)
Mình gộp chung câu a và b để tính đó
Gọi CTHH của hợp chất là TxOy, theo quy tắc hóa trị ta có:
III*x=II*y→x/y=2/3→x=2, y=3
Vậy CTHH của hợp chất lầ T2O3
NTK của hợp chất là: \(\frac{16.3.100\%}{\left(100\%-53\%\right)}=102\)
NTK của T là :\(\frac{102-16.3}{2}=27\)
Vậy T là n tố Al
cho mình hỏi sao bạn lại chia 2 ở câu NTK của T vậy . cảm ơn