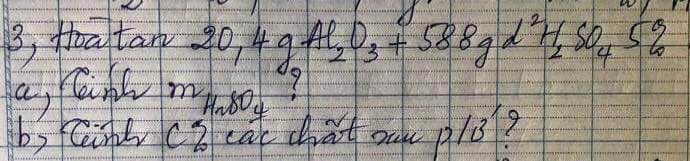Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 12:
PTHH : Cu + H2SO4 --> ( ko Xảy Ra)
Zn +H2SO4---> ZnSO4 + H2
- nH2 = 2.24/22.4 = 0.1 mol
theo PTHH : nZn = nH2 = 0.1 mol
- mZn = 0.1 x 65 =6.5 g
ta có mzn +mCu =m hỗn hợp
=> mCu = 4g
Vậy ...
Câu 10 :
Cho dd HCl tác dụng với hỗn hợp chất rắn Zn và Fe thu được Cu
Zn + 2HCl --> ZnCL2 +H2 (1)
Fe + 2HCl --> FeCl2 +H2 (2)
câu 8 :
-Xét màu của các lọ dd mất nhãn thấy dd có màu xanh là CuCl2 , dd có màu đỏ nâu là FeCl3 ,còn lại 3 dd có màu trắng
- Nhúng quỳ tím vào 3 dd còn lại ta thấy NaOH làm quỳ tím chuyển xanh , HCl làm quỳ tím chuyển đỏ , còn lại NaCl ko có hiện tượng.
câu7:
- Thuốc thử là quỳ tím
-Dùng quỳ tím nhúng vào 4 lọ dd ko màu ta thấy quỳ tím chuyển đỏ là HCl còn lại 3 dd ko có hiện tượng
- dùng dd HCl vừa nhận đc tác dụng với 3 dd AgNO3 , NaNO3, NaCl xét phản ứng ta thấy dd nào xuất hiện kết tủa đó là AgNO3 còn lại 2 dd ko có hiện tượng ( tra bản tính tan trong sgk hóa )
AgNO3 +HCl ---> AgCl +HNO3 (1)
- Cho AgNO3 vào 2 chất còn lại chất nào xuất hiện kết tủa trắng đó là NaCl còn lại là NaNO3 ko có phản ứng
AgNO3 + NaCl ---> AgCl +NaNO3 (2)
~ Tích cho mình nhé ~ (///^.^\\\)

d) Gọi x,y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=8,3\\1,5x+y=0,25\end{matrix}\right.\)
=> x=0,1 ; y=0,1
Kết tủa : Al(OH)3, Fe(OH)2
Bảo toàn nguyên tố Al: \(n_{Al\left(OH\right)_3}=n_{Al}=0,1\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{Fe\left(OH\right)_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(m=0,1.78+0,1.90=16,8\left(g\right)\)
Nung kết tủa thu được chất rắn : Al2O3 và FeO
Bảo toàn nguyên tố Al: \(n_{Al_2O_3}.2=n_{Al}\Rightarrow n_{Al_2O_3}=0,05\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{FeO}=n_{Fe}=0,1\left(mol\right)\)
=> \(a=0,05.102+0,1.72=12,3\left(g\right)\)

Câu 92:
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ ZnO+2HCl\to ZnCl_2+H_2O\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ \Rightarrow n_{Zn}=0,1(mol)\\ \Rightarrow m_{Zn}=0,1.65=6,5(g)\\ \Rightarrow \%_{Zn}=\dfrac{6,5}{14,6}.100\%\approx44,52\%\\ \Rightarrow \%_{ZnO}=100\%-44,52\%=55,48\%\\ b,m_{ZnO}=14,6-6,5=8,1(g)\\ \Rightarrow n_{ZnO}=\dfrac{8,1}{81}=0,1(mol)\\ \Rightarrow \Sigma n_{HCl}=2n_{Zn}+2n_{ZnO}=0,4(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,4}{0,5}=0,8(mol)\)
Câu 93:
\(n_{H_2}=\dfrac{16,8}{22,4}=0,75(mol)\\ PTHH:Fe+H_2SO_4\to FeSO_4+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=0,75(mol)\\ \Rightarrow m_{Fe}=0,75.56=42(g)\\ b,n_{H_2SO_4}=n_{H_2}=0,75(mol)\\ \Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,75}{0,25}=3M\\ c,n_{FeSO_4}=0,75(mol)\\ \Rightarrow m_{CT_{FeSO_4}}=0,75.152=114(g)\\ V_{dd_{FeSO_4}}=V_{dd_{H_2SO_4}}=250(ml)\\ \Rightarrow m_{dd_{FeSO_4}}=250.1,1=275(g)\\ \Rightarrow C\%_{FeSO_4}=\dfrac{114}{275}.100\%\approx41,45\%\)
\(d,m_{FeSO_4.5H_2O}=242.0,75=181,5(g)\)

Bài 11:
\(PTHH:2A+Cl_2\rightarrow2ACl\\TheoĐLBTKL:\\ m_A+m_{Cl_2}=m_{ACl}\\ \Leftrightarrow 9,2+m_{Cl_2}=23,4\\ \Rightarrow m_{Cl_2}=23,4-9,2=14,2\left(g\right)\\ n_{Cl_2}=\dfrac{14,2}{71}=0,2\left(mol\right)\\ n_A=2.0,2=0,4\left(mol\right)\\ M_A=\dfrac{9,2}{0,4}=23\left(\dfrac{g}{mol}\right)\\ \Rightarrow A\left(I\right):Natri\left(Na=23\right)\)

- NaHCO3: Tạo ra khí CO2 tan ít trong nước--> Thỏa mãn
\(2NaHCO_3\underrightarrow{t^o}Na_2CO_3+CO_2+H_2O\)
- NH4Cl và CaO: Tạo ra khí NH3, HCl tan nhiều trong nước --> không thỏa mãn
\(NH_4Cl\underrightarrow{t^o}NH_3+HCl\)
- CH3COONa, NaOH, CaO: Tạo khí CH4 tan ít trong nước --> Thỏa mãn
\(CH_3COONa+NaOH\underrightarrow{t^o,CaO}CH_4+Na_2CO_3\)
- KMnO4: Tạo khí O2 tan ít trong nước --> Thỏa mãn
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)

1)
A là \(CH_2=CH-CH_2OH\)
B là \(CH_2=CH-CHO\)
C là \(CH_2=CH-COOH\)
PTHH:
\(2CH_2=CH-CH_2OH+2Na\rightarrow2CH_2=CH-CH_2ONa+H_2\)
\(2CH_2=CH-COOH+2Na\rightarrow2CH_2=CH-COONa+H_2\)
\(CH_2=CH-CH_2OH+H_2\underrightarrow{t^o,Ni}CH_3-CH_2-CH_2OH\)
\(CH_2=CH-CHO+2H_2\underrightarrow{t^o,Ni}CH_3-CH_2-CH_2OH\)
\(CH_2=CH-CH_2OH+CuO\underrightarrow{t^o}CH_2=CH-CHO+H_2O+Cu\)
2)
TN1:
- Hiện tượng: Sau 1 thời gian, màu vàng của clo nhạt dần. Cho nước vào bình, lắc nhẹ rồi thêm vào bình 1 mẩu giấy quỳ tím thấy giấy chuyển màu đỏ.
- Mục đích: Chứng minh metan pư với clo khi có ánh sáng
\(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
TN2:
- Hiện tượng: dd Br2 nhạt màu dần
- Mục đích: Chứng minh C2H2 pư với Br2
\(C_2H_2+Br_2\rightarrow C_2H_2Br_2\)
\(C_2H_2Br_2+Br_2\rightarrow C_2H_2Br_4\)
TN3:
- Hiện tượng: 2 chất lỏng tạo thành dd đồng nhất
- Mục đích: Chứng minh benzen có thể hòa tan dầu ăn
3)
- Có 3 đồng phân đơn chức mạch hở ứng với CTPT C3H6O2 là C2H5COOH, HCOOC2H5, CH3COOCH3
- C2H5COOH:
\(2CH_4\underrightarrow{1500^oC,làm.lạnh.nhanh}CH\equiv CH+3H_2\)
\(CH\equiv CH+H_2\underrightarrow{t^o,Pd/PbCO_3}CH_2=CH_2\)
\(CH_2=CH_2+HBr\rightarrow CH_3-CH_2Br\)
\(CH_3-CH_2Br+KCN\rightarrow CH_3-CH_2CN+KBr\)
\(CH_3-CH_2CN+2H_2O+H^+\underrightarrow{t^o}CH_3-CH_2-COOH+NH_4^+\)
- HCOOC2H5
\(CH_2=CH_2+H_2O\underrightarrow{t^o,H^+}CH_3-CH_2OH\)
\(CH_4+O_2\underrightarrow{t^o,xt}HCHO+H_2O\)
\(2HCHO+O_2\underrightarrow{t^o,xt}2HCOOH\)
\(HCOOH+CH_3-CH_2OH\underrightarrow{t^o,H^+}HCOOCH_2-CH_3+H_2O\)
- CH3COOCH3
\(C_2H_5OH+O_2\underrightarrow{men.giấm}CH_3COOH+H_2O\)
\(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
\(CH_3Cl+NaOH\rightarrow CH_3OH+NaCl\)
\(CH_3COOH+CH_3OH\underrightarrow{t^o,H^+}CH_3COOCH_3+H_2O\)
4)
- Trích một ít các chất làm mẫu thử, hòa tan các chất vào nước:
+ Chất lỏng tan, tạo thành thể đồng nhất: C2H5COOH
+ Chất lỏng không tan, tách thành 2 lớp: HCOOC2H5, CH3COOCH3 (1)
- Cho các chất ở (1) tác dụng với dd AgNO3/NH3, đun nóng:
+ Xuất hiện kết tủa trắng xám bám vào ống nghiệm: HCOOC2H5
\(HCOOC_2H_5+2AgNO_3+3NH_3+H_2O\underrightarrow{t^o}2Ag+2NH_4NO_3+NH_4OCOOC_2H_5\)
+ Không hiện tượng: CH3COOCH3

PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Ta có: \(\left\{{}\begin{matrix}m_{H_2SO_4}=588\cdot5\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,3}{3}\) \(\Rightarrow\) Al2O3 còn dư
\(\Rightarrow n_{Al_2\left(SO_4\right)_3}=0,1\left(mol\right)=n_{Al_2O_3\left(dư\right)}\)
\(\Rightarrow C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1\cdot342}{20,4+588-0,1\cdot102}\cdot100\%\approx5,72\%\)

nSO3=8/80=0,1(mol)
pthh: SO3 + H2O -> H2SO4
nH2SO4=nSO3=0,1(mol) => mH2SO4(tạo sau)= 0,1.98=9,8(g)
mH2SO4(tổng)= 100.9,8% + 9,8=19,6(g)
mddH2SO4(sau)=8+100=108(g)
=>C%ddH2SO4(sau)= (19,6/108).100=18,148%

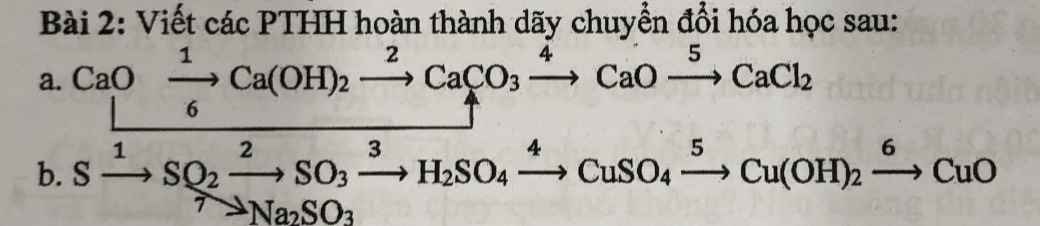
Bài 2 :
a) (1) \(CaO+CO_2\rightarrow CaCO_3\)
(2) \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
(3) \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
(4) \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
(5) \(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Chúc bạn học tốt
b)(1) \(S+O_2\underrightarrow{t^o}SO_2\)
(2) \(2SO_2+O_2\underrightarrow{t^o,V_2O_5}2SO_3\)
(3) \(SO_3+H_2O\rightarrow H_2SO_4\)
(4) \(H_2SO_4+CuO\rightarrow CuSO_4+H_2O\)
(5) \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
(6) \(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
(7) \(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
Chúc bạn học tốt




 Mk đang cần gấp, mn giúp mình vs ạ
Mk đang cần gấp, mn giúp mình vs ạ