Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: BaCl2 + H2SO4 -> BaSO4 (kt trắng) + 2HCl
Mô tả hiện tượng: Có kết tủa trắng tạo thành sau phản ứng.
Giải thích: BaCl2 tác dụng với H2SO4 theo tính chất của muối và axit, tạo muối BaSO4 không tan (kết tủa trắng) và dung dịch HCl.

PTHH: Na2CO3 + CaCl2 -> CaCO3 (kết tủa trắng) + 2NaCl
Hiện tượng: Có kết tủa trắng sau phản ứng.
Giải thích: Na2CO3 tác dụng với CaCl2 tạo muối CaCO3 không tan (kt trắng) và dd NaCl.

Hiện tượng :
- Viên kẽm tan dần trong dd HCl loãng, có khí không màu thoát ra.
- Dấu hiệu chứng tỏ có phản ứng hoá học giữa HCl và Zn là mẩu Zn tan dần, có khí thoát ra.

PTHH: CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
Hiện tượng: Dung dịch CuSO4 mất màu xanh, có kết tủa xanh lam sau phản ứng
Giải thích: ion Cu2+ có tác dụng với ion OH- tạo kết tủa xanh lam Cu(OH)2

- Lượng bót khí thoát ra ở bình số 2 nhiều hơn bình số 1.
Nhận xét :
- Dd có nồng độ càng cao thì tốc độ phản ứng cao lên và mạnh hơn.
Giải thích :
Khi nồng độ tăng thì tốc độ phản ứng tăng. Do khi nồng độ các chất tham gia phản ứng tăng thì số phần tử hoạt động có trong một đơn vị thể tích tăng dẫn đến số va chạm có hiệu quả tăng → tốc độ phản ứng tăng.

- Phản ứng ở ống nghiệm (2) xảy ra nhanh hơn.
- Khi tăng nồng độ chất tham gia phản ứng thì tốc độ phản ứng tăng.

Hiện tượng: Dung dịch NaOH chuyển sang màu hồng, dung dịch HCl không thay đổi màu sắc.
Giải thích: dd NaOH có tính base bị phenolphthalein làm dung dịch base chuyển sang màu hồng nhạt, dung dịch HCl có tính acid không có tính chất làm chuyển màu dung dịch nhờ phenolphthalein nên giữ được màu sắc ban đầu.

- Đường trước khi đun: Lúc đầu đường là chất rắn, có màu trắng, có vị ngọt, không có mùi, dễ bị tan trong nước.
- Đường sau khi đun đường cũng vẫn là chất rắn nhưng có màu đen, có vị đắng hơn so với đường ban đầu, mùi khét, không tan trong nước.
- Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra: nó đã thay đổi màu sắc, thay đổi mùi vị của chúng và cả tan hay ko tan trong nước.
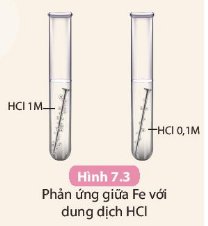


Hiện tượng:
- Đinh sắt tan dần trong dd H2SO4 loãng và có chất khí không màu thoát ra.
- Chiếc đinh sắt bên ống nghiệm 1 tan nhanh hơn và p/ư xảy ra dữ dội hơn.
Nhận xét:
- Nhiệt độ cao làm tăng tốc độ phản ứng.