Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
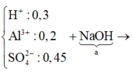
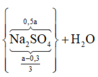
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

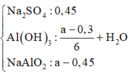
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
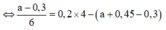
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C

Đáp án C
Trong 400 ml dung dịch E có :
![]()
![]()
![]()
⇔ n OH - ban đầu > n OH - / Al OH 3
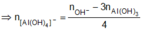
= 0,072 mol
Vậy trong phản ứng của E với dung dịch NaOH đã có hiện tượng hòa tan một phần kết tủa.
Áp dụng bảo toàn điện tích trong dung dịch G, ta có :
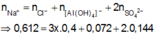
![]()
Suy ra : x:y = 0,21:0,12 = 7:4

Đáp án A
Dung dịch sau phản ứng chắc chắn có chứa các ion K + , Na + , Cl - . Mặt khác, n K + + n Na + > n Cl - , suy ra dung dịch sau phản ứng còn chứa ion âm, đó là Al OH 4 - . Theo bảo toàn điện tích, ta có :

![]()
![]()
= 0,05 mol
![]()

Chọn đáp án B
Ta có: 1 mol dung dịch X chứa x+2y mol OH-
+ Ta có 1 mol dung dịch Y chứa y+2x mol OH-
+ Vì khi cho SO42- vào vẫn còn kết tủa nên lượng kết tủa tính trong bài hoàn toàn tính theo CO32-
+ Hấp thụ hết 0,04 mol CO2 vào 200 ml dung dịch X, thu được dung dịch M và 1,97 gam kết tủa
⇒ nOH– = 0,2×(x+2y)
⇒ nBaCO3 = 0,01, nBa(HCO3)2 = 0 , 04 - 0 , 01 2 = 0,015 mol
⇒ nOH– = 0,01×2 + 0,015×2 = 0,05 mol.
⇒ x + 2y = 0,25.
+ Nếu hấp thụ hết 0,0325 mol CO2 vào 200 ml dung dịch Y thì thu được dung dịch B và 1,4775 gam kết tủa.
nBaCO3 = 0,0075 ⇒ nHCO3– = 0,0325 – 0,0075 = 0,025.
⇒ nOH– = 0,2×(2x + y) = 0,025 + 0,0075×2 = 0,04 → 2x + y = 0,2.
⇒ x = 0,05 và y = 0,1

Đáp án B
Kết tủa là BaCO3: n B a C O 3 = 0,08 mol
Cho từ từ HCl 1M vào X thì khi bắt đầu có khí thì cần 0,12 mol HCl
TH1 có tạo thành NaHCO3 → X chứa 0,12 mol Na2CO3 do vậy Ba đi hết vào kết tủa
![]()
TH2: có NaOH dư → X chứa NaOH và Na2CO3 với tổng số mol là 0,12 và Ba đi hết vào kết tủa
=> n N a O H = 0,02 mol
Giải được số mol NaOH dư và Na2CO3 lần lượt là 0,04 và 0,08 mol
Bảo toàn C: a=0,16 mol
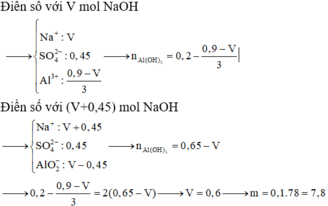



Đáp án D