Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi $n_{Cu} = a(mol) ; n_{Al} = b(mol) \Rightarrow 64a + 27b = 3(1)$
$Cu^0 \to Cu^{+2} + 2e$
$Al^0 \to Al^{+3} + 3e$
$N^{+5} + 1e \to N^{+4}$
Bảo toàn electron :
$2a + 3b = 0,2(2)$
Từ (1)(2) suy ra $a = \dfrac{3}{115} ; b = \dfrac{17}{345}$
\(\%m_{Cu}=\dfrac{\dfrac{3}{115}.64}{3}.100\%=55,65\%\\ \%m_{Al}=100\%-55,65\%=44,35\%\)
Gọi số mol của Cu và Al lần lượt là x,y (mol) (x,y>0)
\(Cu+4HNO_{3\left(đ\right)}\underrightarrow{to}Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ x..................................2x\left(mol\right)\\ Al+6HNO_{3\left(đ\right)}\underrightarrow{to}Al\left(NO_3\right)_3+3NO_2+3H_2O\\ y...............................3y\left(mol\right)\)
\(\left\{{}\begin{matrix}64x+27y=3\\2x+3y=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=\dfrac{3}{115}\\y=\dfrac{17}{345}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{\dfrac{3}{115}.64}{3}.100\approx55,652\%\\\%m_{Al}\approx44,348\%\end{matrix}\right.\\ \)

Gọi nAl = x (mol), nCu = y (mol); nNO2 = 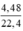 = 0,2 mol
= 0,2 mol
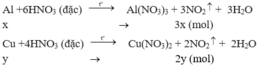
Theo pt: nNO2(1) = 3. nAl = 3.x mol
nNO2(2) = 2. nCu = 2y mol
⇒ Tổng nNO2 = 3x + 2y = 0,2 mol
Ta có hệ phương trình
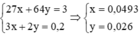
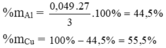

QT cho e: Xét với ½ khối lượng hỗn hợp
Mg→ Mg2++ 2e (1)
x 2x mol
Al→ Al3++ 3e (2)
y 3y mol
Cu→ Cu2++ 2e (3)
z 2z mol
→ne cho= 2x+ 3y+2z mol
QT nhận e:
-Phần 1: nNO2=0,47 mol
N+5+ 1e→ NO2
0,47 0,47 mol
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
-Phần 2:
Cl2+ 2e→ 2Cl-
0,47 0,47
Theo ĐL bảo toàn e: ne cho= 2x+ 3y+2z = ne nhận= 0,47
mmuối clorua= mkim loại+ mCl-= mkim loại+ 0,47.35,5=27,875 → mkim loại=11,19 gam → m= 11,19.2=22,38 gam

\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=6.95\left(g\right)\left(1\right)\)
\(n_{NO_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
Bảo toàn e :
\(3a+3b=0.45\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.05,b=0.1\)
\(m_{Al}=0.05\cdot27=1.35\left(g\right)\)
\(m_{Fe}=0.1\cdot56=5.6\left(g\right)\)

Đặt: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\) (x,y: nguyên, dương)
PTHH: Fe + 4 HNO3 -> Fe(NO3)3 + NO + 2 H2O
x_____________________________x(mol)
3 Cu + 8 HNO3 ->3 Cu(NO3)2 + 2 NO + 4 H2O
y_________________________2/3y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}56x+64y=12,4\\x+\dfrac{2}{3}y=0,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
=>mFe=0,05.56=2,8(g)
=>%mFe=(2,8/12,4).100=22,581%
=>%mCu= 77,419%

Gọi $n_{Fe} = a(mol) ; n_{Zn} = b(mol) \Rightarrow 56a + 65b = 1,77(1)$
$n_{NO_2} = \dfrac{1,792}{22,4} = 0,08(mol)$
Bảo toàn electron :
$3n_{Fe} + 2n_{Zn} = n_{NO_2} \Rightarrow 3a + 2b = 0,08(2)$
Từ (1)(2) suy ra: a = 0,02 ; b = 0,01
$\%m_{Fe} = \dfrac{0,02.56}{1,77}.100\% = 63,3\%$
$\%m_{Zn} =100\% - 63,3\% = 36,7\%$

Ag + 2HNO3 ⟶ AgNO3 + H2O + NO2
Cu + 4HNO3 → Cu(NO3)2 + 2H2O + 2NO2
Gọi x,y lần lượt là số mol Ag, Cu
\(\left\{{}\begin{matrix}108x+64y=30\\x+2y=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,27\\y=0,016\end{matrix}\right.\)
=> \(\%m_{Cu}=\dfrac{0,016.64}{30}.100=3,41\%\)
$n_{NO_2} = 0,13(mol)$
$n_{Zn} = a(mol) ; n_{Al} = b(mol)$
Ta có :
$m_{hh} = 65a + 27b = 2,11(gam)$
Bảo toàn electron : $2a + 3b = 0,13$
Suy ra a = 0,02 ; b = 0,03
$\%m_{Zn} = \dfrac{0,02.65}{2,11}.100\% = 61,61\%$
$\%m_{Al} = 100\% -61,61\% = 38,39\%$