Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
n C l 2 = 1 , 12 22 , 4 = 0,05 (mol); n N a O H d ư = 0,2.0,5 = 0,1 (mol)
C l 2 + 2NaOH → NaCl + NaClO + H 2 O
0,05 0,1 (mol)
=> n N a O H b đ = 0,1 + 0,1 = 0,2 (mol) => C M N a O H = = 1,0 (M)

Đáp án D
Lượng muối KCl sinh ra trong hai dung dịch bằng nhau, giả sử là a mol.
Cl2 + 2KOH → KCl + KClO + H2O (1)
a ← a
3Cl2 + 6KOH ![]() 5KCl + KClO3 + 3H2O (2)
5KCl + KClO3 + 3H2O (2)
3a/5 ← a
Tỉ lệ thể tích khí clo đi qua dung dịch thứ nhất và thứ 2 là = 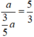

Đáp án D
Gọi số mol HCl là x mol
HCl + KOH → KCl + H2O
x x (mol)
Giả sử KOH hết ⇒ mKCl = 74,5 . 0,1 = 7.45(g) > 6,525 ⇒KOH dư ,HCl hết.
(0,1 - x).56 + x.(39 + 35,5) = 6,525
⇒ x = 0,05 mol ⇒ CM = 0,5M

\(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=5,6\left(g\right)\)
\(\Rightarrow m_{Fe_2O_3}=16\left(g\right)\)
\(\Rightarrow n_{Fe}=2n_{Fe_2O_3}=0,2\left(mol\right)=n_{FeCl_3}\)
Lại có : \(n_{HCl}=2n_{H_2}+3n_{FeCl_3}=0,8\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=292\left(g\right)\)
\(\Rightarrow V=\dfrac{2920}{11}\left(ml\right)=\dfrac{73}{275}\left(l\right)\)
\(\Rightarrow C_{MFeCl_3}=\dfrac{0,2}{\dfrac{73}{275}}=\dfrac{55}{73}\left(M\right)\)

Đáp án A
nKOH = 0,1.1=0,1 (mol)
KOH + HCl →KCl + H2O
0,1→ 0,1 (mol)
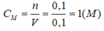

Đổi: 400ml = 0,4l
nHCl = CM.V = 0,4 (mol)
Pthh:
FeO + 2HCl -> FeCl2 + H2O
0,025 0,05 0,025
CaCO3 + 2HCl -> CaCl2 + H2O + CO2
0,1 0,2 0,1 0,1
nCO2 = V/22,4 = 2,24/22,4 = 0,1 (mol)
=> mCaCO3 = M.n = 100 x 0,1 = 10 (g)
=> mFeO = 1,8 (g) => nFeO = 0,025 (mol)
=> nHCl(dư) = 0,4 - 0,2 - 0,05 = 0,15 (mol)
+) CMHCl(dư) = n/V = 0,15/0,4 = 0,375 mol
+) CMFeCl2 = n/V = 0,025/4 = 0,0625 mol
+) CMCaCl2 = n/V = 0,1/4 = 0,25 mol

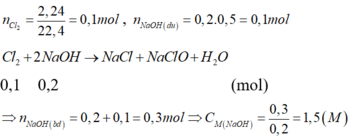
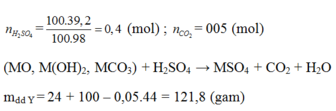
Câu 5 : Cho hỗn hợp hai muối MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 2,24 lít khí đktc . Số mol của 2 muối cacbonat ban đầu là ?
CaCO3-->CaO+CO2
n hỗn hợp khí =2,24\22,4 =0,1 mol
=>nhh 2muối =0,1 mol
câu4
Gọi số mol HCl là x mol
HCl + KOH → KCl + H2O
x x (mol)
Giả sử KOH hết ⇒ mKCl = 74,5 . 0,1 = 7.45(g) > 6,525 ⇒KOH dư ,HCl hết.
(0,1 - x).56 + x.(39 + 35,5) = 6,525
⇒ x = 0,05 mol ⇒ CM = 0,5M