- Phần 1: Tan hoàn toàn trong dung dịch HCl giải phóng V lít khí ở đktc và tạo 16,02g hỗn hợp muối chloride
- Phần 2: Bị oxi hóa hoàn toàn thu được m gam hỗn hợp 3 oxide.
Giá trị V và m lần lượt là:
A. 4,032 và 6,12
B. 4,032 và 5,96
C. 8,64 và 6,12
D. 8,64 và 5,96
Giải thích giúp e với ạ



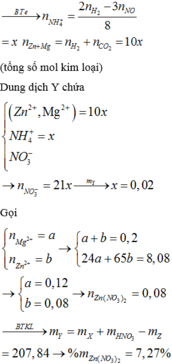
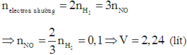


Ta có: mKL (trong 1 phần) = 6,48:2 = 3,24
- Phần 1:
m muối = mKL + mCl- \(\Rightarrow n_{Cl^-}=\dfrac{16,02-3,24}{35,5}=0,36\left(mol\right)\)
BTNT Cl: nHCl = nCl- = 0,36 (mol)
BTNT H: nH2 = 1/2nHCl = 0,18 (mol)
\(\Rightarrow V_{H_2}=0,18.22,4=4,032\left(l\right)\)
- Phần 2:
BT e, có: 2nZn + 2nMg + 3nAl = 2nH2 = 4nO2
⇒ nO2 = 0,09 (mol)
⇒ m oxide = mKL + mO2 = 3,24 + 0,09.32 = 6,12 (g)