Cho19,5gam znic tác dụng với hydrocloric acid a: tính thể tích (đktc) b:nếu dùng khí trên khử 19,2 gam iron(III) axit thì mIron =?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH :
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,3 0,3
\(a,V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(b,PTHH:\)
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
trc p/u: 0,3 0,12
p/u: 0,3 0,1 0,2 0,3
sau : 0 0,02 0,2 0,3
----> Fe2O3 dư
\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
\(n_{Fe}=0,2.56=11,2\left(g\right)\)

Bài 13:
a) \(n_{H_2}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0,2---------------------------->0,3
=> VH2 = 0,3.24,79 = 7,437 (l)
b)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,3------->0,2
=> mFe = 0,2.56 = 11,2 (g)

a.\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.24,79=7,437l\)
b.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,3 0,2 ( mol )
\(m_{Fe}=0,2.56=11,2g\)

Bài 1:
a, \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.24,79=7,437\left(l\right)\)
b, \(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,12}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
Bài 2:
Ta có: \(n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.24,79=4,958\left(l\right)\)
\(n_{NaOH}=n_{Na}=0,4\left(mol\right)\Rightarrow m_{NaOH}=0,4.40=16\left(g\right)\)

PTHH: Zn + 2HCl → ZnCl2 + H2 ↑
Số mol của Zn là: 19,5 : 65 = 0,3 mol
Số mol của H2 là: 0,3 . 1 = 0,3 mol
a) Thể tích H2 thu được là: 0,3 . 22,4 = 6,72 lít
b) PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Số mol của Fe2O3 là: 19,2 : 160 = 0,12 mol
So sánh: \(\frac{0,3}{3}< 0,12\) => Fe2O3 dư, tính theo H2
Số mol của Fe là: 0,3 . 2/3 = 0,2 mol
Khối lượng Fe là: 0,2 . 56 = 11,2 gam
nZn=19,5:65=0,3mol
PTHH: Zn+2HCl=>ZnCl2+H2
0,3->0,6->0,3->0,3
=> V H2=0,3.22,4=6,72ml
thu đc bao nhiêu gam j

\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3
\(V_{H_2}=0,3.22,4=6,72l\\ n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12g\\ pthh:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ LTL:\dfrac{0,12}{1}>\dfrac{0,3}{3}\)
=> Fe2O3 dư
\(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\\
m_{Fe}=0,2.56=11,2g\)
a.\(n_{Zn}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,12 > 0,3 ( mol )
0,3 0,2 ( mol )
\(m_{Fe}=0,2.56=11,2g\)
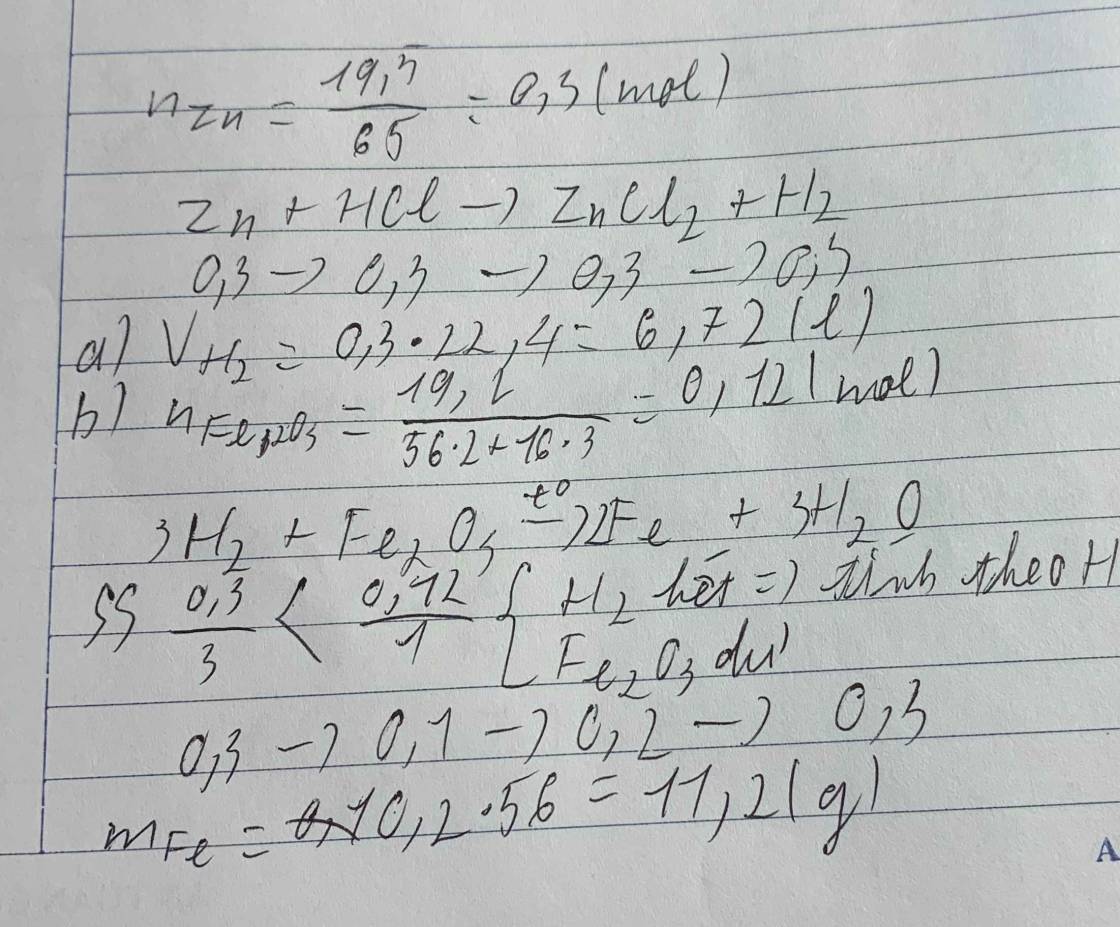
\(a,n_{Zn}=\dfrac{19,5}{65}=0,3mol\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,3mol\\ V_{H_2}=0,3.24,79=7,437l\\ b,FeO+H_2\xrightarrow[t^0]{}Fe+H_2O\\ n_{FeO}=\dfrac{19,2}{72}=\dfrac{4}{15}mol\\ \Rightarrow\dfrac{0,3}{1}>\dfrac{4:15}{1}\Rightarrow H_2.dư\\ n_{Fe}=n_{FeO}=\dfrac{4}{15}mol\\ m_{Fe}=\dfrac{4}{15}.56\approx14,93g\)
Cho mình hỏi ở Vh2: sao lại có 22,4 v ạ