6:2. Hòa tan hết m gam hỗn hợp (X) gồm Fe và Fe2O3 bằng dung dịch chứa H2SO4 thu được 3,584 lít khí SO2 đo đktc (không còn sản phẩm khử nào khác) và dung dịch (Y) chứa muối và axit dư. Chia dung dịch Y thành hai phần bằng nhau. Phần một tác dụng với 500 ml dung dịch KOH 0,4M, thu được 5,35 gam một chất kết tủa. Phần hai tác dụng với dung dịch Ba(OH) 2 dư, thu được 42,345 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. )Viết phản ứng hóa học xảy ra 6.2b) Tính giá trị m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
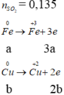
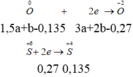
mX = 56a+64b+16(1,5a+b-0,135) = 38,64
=> 80a + 80b = 40,8 (1)
mmuối sunfat = 200a + 160b = 99,6
=> a = 0,45; b=0,06

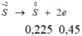
m ↓ = 0,225.32 + 0,06.96 = 12,96 (g)

H2SO4 dùng dư đề cho rõ ràng nhé → 21,4 gam kết tủa rõ là 0,2 mol Fe(OH)3.
mà có 0,9 mol NaOH → chứng tỏ nH+ trong Y = 0,3 mol. hết.!
(p/s: đừng nhầm lẫn 0,2 mol Fe(OH)3 → ∑nFe trong X = 0,2 luôn nhé.!).
♦ CB3: 19,2 gam (Fe; O) + 0,75 mol H2SO4 (lượng đủ) → Fe2(SO4)3 + SO2 + H2O.
có 2x mol Fe → x mol Fe2(SO4)3
→ nSO2 = 0,75 – 3x theo bảo toàn S.
bảo toàn electron có 2nO trong X = 3nFe – 2nSO2
→ nO trong X = 6x – 0,75 mol
||→ mX = mFe + mO = 56 × 2x + 16 × (6x – 0,75) = 19,2
→ giải ra: x = 0,15 mol.
→ nSO2 = 0,75 – x = 0,3 mol → Yêu cầu VSO2 = 6,72 lít.
p/s: giải CB3 có khá nhiều hướng khác: ví dụ gọi x như trên thì có SO2 theo x;
nH2O = 0,375 mol → BTKL cả phương trình giải ra x luôn.!
Đáp án B

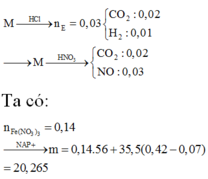
Đáp án A
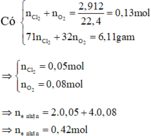
Y + HCl => Z chỉ chứa hai muối, HCl phản ứng hết
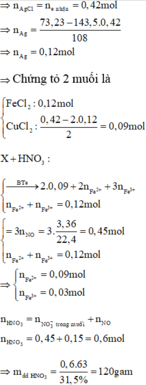
⇒ m dd T = 120 + 64 . 0 , 09 + 56 . 0 , 12 - 30 . 0 , 15 = 127 , 98 gam ⇒ C % Fe NO 3 3 = 242 . 0 , 03 127 , 98 . 100 % = 5 , 67 %
gần với giá trị 5% nhất
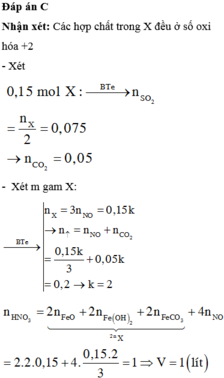

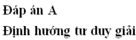

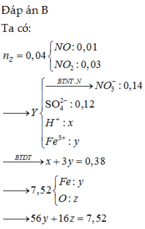
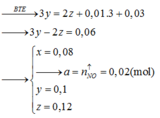


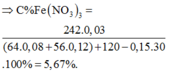
a, \(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Y gồm: Fe2(SO4)3 và H2SO4 dư.
- Phần 1: \(Fe_2\left(SO_4\right)_3+6KOH\rightarrow3K_2SO_4+2Fe\left(OH\right)_3\)
\(H_2SO_4+2KOH\rightarrow K_2SO_4+2H_2O\)
- Phần 2: \(Fe_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow3BaSO_4+2Fe\left(OH\right)_3\)
___________x_________________________3x_______2x (mol)
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
b, \(n_{SO_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
BT e, có: 3nFe = 2nSO2 ⇒ nFe = 8/75 (mol)
- Phần 1:
\(n_{KOH}=0,5.0,4=0,2\left(mol\right)\)
\(n_{Fe\left(OH\right)_3}=\dfrac{5,35}{107}=0,05\left(mol\right)\)
Theo PT: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_3}=0,025\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{0,2-0,15}{2}=0,025\left(mol\right)\)
- Phần 2: m kết tủa = mBaSO4 + mFe(OH)3
⇒ 42,345 = 0,025.233 + 3x.233 + 2x.107
⇒ x = 0,04
→ Trong 1 phần có: nFe2(SO4)3 = 0,04 (mol), nH2SO4 = 0,025 (mol)
BTNT Fe, có: nFe + 2nFe2O3 = 2nFe2(SO4)3
⇒ 8/75 + 2nFe2O3 = 2.0,04.2
⇒ nFe2O3 = 2/75 (mol)
⇒ m = 10,24 (g)