Mô tả liên kết hóa học trong phân tử SiH4 theo thuyết lai hóa
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a,\) Gọi ct chung: \(C^{IV}_xO^{II}_y\)
Theo qui tắc hóa trị: \(IV.x=y.II\Rightarrow\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{1}{2}\)
\(\Rightarrow x=1;y=2\)
\(\Rightarrow CTHH:CO_2\)
\(b,\) Khi hình thành phân tử Carbon dioxide, 2 nguyên tử O đã liên kết với 1 nguyên tử C bằng cách nguyên tử C góp chung 2 electron với mỗi nguyên tử O để tạo thành cặp electron dùng chung.
*Hình ảnh về cấu tạo của phân tử nhé.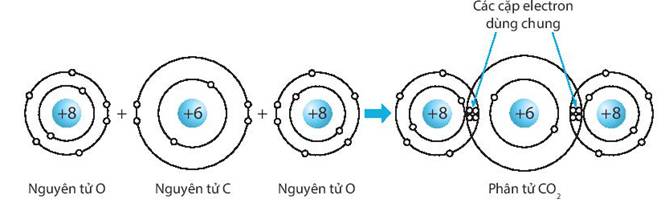

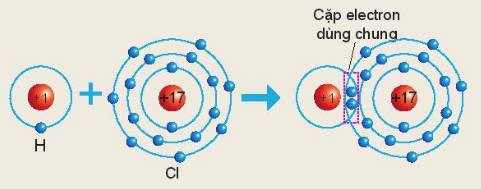
Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.

`-` Khi hình thành liên kết cộng hóa trị trong phân tử `CO_2`, các nguyên tử đã liên kết với nhau như sau:
Mỗi nguyên tử `C` và `O` lần lượt có `12e` và `16e`. Để hình thành phân tử `CO_2`, nguyên tử `C` đã liên kết với `2` nguyên tử `O` bằng cách nguyên tử `C` góp chung với mỗi nguyên tử `O` là `2e` ở lớp ngoài cùng tạo thành các cặp electron dùng chung.
`NH_3`
Mỗi nguyên tử `N` và `H` lần lượt có `14e` và `1e`. Để hình thành phân tử ammonia, nguyên tử `N` liên kết với nguyên tử `H` bằng cách nguyên tử `N` góp chung với nguyên tử `H` là `1e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.

Khi tạo thành phân tử nước, nguyên tử O góp 2 electron, mỗi nguyên tử H góp 1 electron. Như vậy, giữa nguyên tử O và nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử O và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử nước.

`Cl_2`
Mỗi nguyên tử `Cl` có `7e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ar`, `2` nguyên tử `Cl` đã liên kết với nhau bằng cách mỗi nguyên tử `Cl` góp chung `1e` ở lớp ngoài cùng tạo thành `1` cặp electron dùng chung.
`N_2`
Mỗi nguyên tử `N` có `5e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ne`,`2` nguyên tử `N` đã liên kết với nhau bằng cách mỗi nguyên tử `N` góp chung `3e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.

- Quá trình tạo thành liên kết cộng hóa trị trong phân tử hydrogen:
+ Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử H liên kết với nhau, mỗi nguyên tử góp chung 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử H cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử hydrogen.
- Quá trình tạo thành liên kết cộng hóa trị trong phân tử oxygen:
+ Nguyên tử O có 6 electron lớp ngoài cùng, cần thêm 2 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử O liên kết với nhau, mỗi nguyên tử góp 2 electron để tạo ra hai cặp electron dùng chung.
+ Hạt nhân của hai nguyên tử O cùng hút các cặp electron dùng chung và liên kết với nhau tạo thành phân tử oxygen.
\(_{14}Si:\left[Ne\right]3s^23p^2->LH:sp^3\)
4 orbital lai hoá của silicon xen phủ với 4 orbital s của 4 nguyên tử hydrogen tạo liên kết sigma, cho phân tử \(SiH_4\)