Phòng thí nghiệm có một lọ đựng dung dịch sulfuric acid đặc không còn nguyên chất, không sử dụng được nữa. Hãy để xuất cách loại bỏ lọ acid này một cách an toàn mà ít gây ảnh hưởng đến môi trường và sức khoẻ.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Trích mẫu thử, cho \(Ba\left(OH\right)_2\) vào các mẫu thử:
+ Tạo dd màu xanh lá và kết tủa trắng là \(CuSO_4\)
- Cho 2 mẫu thử còn lại vào dd \(HCl\):
+ Tạo kết tủa trắng là \(AgNO_3\)
+ Ko ht là \(Na_2SO_4\)
\(PTHH:CuSO_4+BaCl_2\rightarrow CuCl_2+BaSO_4\downarrow\\ AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
Na2SO4 + Ba(OH)2 cho kết tủa trắng chứ nhỉ?

- Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc không phải là benzene (benzene không màu).
- Vì benzene phản ứng với dung dịch nitric acid tạo nitrobenzene có màu vàng nhạt .
PTHH: C6H6 + HNO3 → C6H5NO2 + H2O

a, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd NaCl.
+ Có tủa trắng: AgNO3.
PT: \(AgNO_3+NaCl\rightarrow AgCl_{\downarrow}+NaNO_3\)
+ Không hiện tượng: CuSO4, NaCl. (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2.
+ Có tủa trắng: CuSO4.
PT: \(CuSO_4+BaCl_2\rightarrow BaSO_{4\downarrow}+CuCl_2\)
+ Không hiện tượng: NaCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd BaCl2.
+ Có tủa trắng: H2SO4
PT: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_{4\downarrow}\)
+ Không hiện tượng: HCl
- Dán nhãn.

CuSO4, AgNO3, NaCl
BaCl2 ↓trắng ↓trắng ∅
NaCl ↓nâu ↓trắng sữa
- Lấy mỗi chất một ít cho vào ống nghiệm, đánh STT, sau đó nhỏ dung dịch BaCl2 vào từng ống.
(BaCl2+2AgNO3→Ba(NO3)2+2AgCl ; BaCl2+CuSO4→BaSO4+CuCl2)
+ Thấy xuất hiện kết tủa là AgNO3 và CuSO4 còn lại là NaCl.
- Nhỏ dung dịch NaCl vào 2 dung dịch AgNO3 và CuSO4
+ Xuất hiện kết tủa màu trắng sữa là AgCl chất ban đầu là AgNO3.
( AgNO3 + NaCl ➝ AgCl + NaNO3 )
+ Thấy dung dịch có màu xanh lá cây và có kết tủa màu nâu là CuCl2 và chất ban đầu là CuSO4.
( CuSO4 + NaCl → CuCl2 + Na2SO4 )

Việc sử dụng acid không đúng cách sẽ gây ô nhiễm môi trường đất, nước, không khí. Cụ thể:
- Acid dư thừa sau sử dụng thải trực tiếp ra môi trường ngấm vào đất làm chua đất, làm rửa trôi các chất dinh dưỡng có trong đất … không những thế chúng còn làm cho cây trồng bị suy yếu và chết hàng loạt. Nhất là đối với những cây nông nghiệp (rau, củ, quả …) môi trường acid sẽ gây ra những thiệt hại lớn …
- Acid dư thừa sau sử dụng thải trực tiếp ra môi trường nước làm giảm độ pH của nước, khiến cho các loài sinh vật bị cản trở quá trình hấp thụ chất dinh dưỡng … Ngoài ra, các loài sinh vật sẽ bị hạn chế phát triển, chết dần và khó có thể tái tạo về môi trường sinh thái ban đầu. Đối với những người dân chuyên sống bằng nghề nuôi trồng và đánh bắt thủy hải sản, thì đây sẽ là một mối nguy cơ lớn gây ảnh hưởng tới đời sống kinh tế và sản xuất của người dân.
- Trong không khí các hạt acid lơ lửng gây ô nhiễm không khí, ảnh hưởng tới tầm nhìn xa trong không khí gây cản trở tới hoạt động nghiên cứu của các chuyên gia về khí tượng, môi trường…
- Đối với con người, khi da tiếp xúc với môi trường không khí bị ô nhiễm do acid sẽ gây ra các bệnh về da như mẩn ngứa, nấm, viêm da, gây mụn nhọt, mụn trứng cá… Sử dụng nước dư acid trong ăn uống còn gây ảnh hưởng tới hệ tiêu hóa, gây ra các bệnh về đường ruột như trào ngược dạ dày, đau dạ dày, ợ hơi, khó tiêu… Trẻ em sử dụng nước dư acid thường xuyên sẽ gây tổn hại cho hệ thần kinh, não bộ, thậm chí là tử vong. Về lâu dài, nước dư acid còn là nguyên nhân gây ra bệnh Alzheimer ở người già. Khi hít thở không khí có chứa các hạt bụi acid sẽ làm ảnh hưởng tới đường hô hấp và giảm sức đề kháng của cơ thể….

Cho dung dịch HCl vào các mẫu thử
+ Tan, tạo thành dung dịch có màu xanh lục nhạt, có khí không màu, không mùi, nhẹ hơn không khí thoát ra : Fe
Fe + 2HCl → FeCl2 + H2
+ Tan, tạo thành dung dịch có màu hồng, có khí mùi sốc thoát ra : MnO2
4HCl + MnO2 ⟶ Cl2 + 2H2O + MnCl2
+ Tan, tạo dung dịch trong suốt, khí thoát ra có mùi hắc : Na2SO3
Na2SO3 + 2HCl → 2NaCl + SO2↑ + H2O
+ Tan, tạo thành dung dịch trong suốt, khí không màu thoát ra, nặng hơn không khí : KHCO3
KHCO3 + HCl → KCl + CO2 + H2O
+ Tan, tạo dung dịch màu xanh lục nhạt, khí thoát ra có mùi trứng thối: H2S
FeS + 2HCl → FeCl2 + H2S
+ Không tan : Na2SiO3
Trích mẫu thử:
- Cho dd HCl vào các mẫu thử.
+ Nếu tan, tạo thành dung dịch không màu ( trong suốt ) và có mùi hăng thì là: Na2SO3.
PT: Na2SO3 + 2HCl → 2NaCl + SO2\(\uparrow\) + H2O.
+ Nếu tan, tạo thành dd có màu xanh nước biển nhạt và có khí H2 thoát ra thì là: Fe.
PT: Fe + 2HCl → FeCl2 + H2.
+ Nếu tan, tạo thành dung dịch có màu hồng và có khí sộc vào mũi thì là: MnO2.
PT: MnO2 + 4HCl → MnCl2 + Cl2 + H2O.
+ nếu tan, tạo thành dd trong suốt và có khí CO2 thoát ra thì là: KHCO3.
PT: KHCO3 + HCl → KCl + CO2 + H2O.
+ Nếu tan, tạo thành dd màu xanh nước biển nhạt, có mùi thối thoát ra là: FeS.
PT: FeS + 2HCl → FeCl2 + H2S.
+ Nếu không tan là: Na2SiO3.

- Lấy một phần mỗi dung dịch vào từng ống nghiệm, rồi nhỏ dung dịch HCl vào. Ở ống nghiệm có khí thoát ra là ống đựng dung dịch N a 2 C O 3 .
![]()
- Phân biệt dung dịch H 3 P O 4 , B a C l 2 , ( N H 4 ) 2 S O 4 bằng cách cho N a 2 C O 3 tác dụng với từng dung dịch: dung dịch nào khi phản ứng cho khí thoát ra là H3PO4, dung dịch nào khi phản ứng có kết tủa trắng xuất hiện là B a C l 2 , dung dịch nào khi phản ứng không có hiện tượng gì là ( N H 4 ) 2 S O 4 :
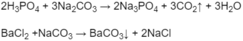

(1) Không dùng tay trực tiếp cầm hóa chất.
(2) Không đổ hóa chất này vào hóa chất khác.
(4) Không dùng hóa chất đựng trong những lọ không có nhãn ghi rõ tên hóa chất.
(5) Không nếm hoặc ngửi trực tiếp hóa chất.
Đáp án B
- Cách loại bỏ: Sử dụng dịch base (nước vôi trong - Ca(OH)2) để trung hòa acid, tạo kết tủa với ion
- Phương trình: