cho 0,50 lít CH4 và C2H4 tác dụng với dung dịch brom dư thì thấy khối lượng brom cần sử dụng là 1.6 gam . tính % theo thể tích của mỗi khí trong hỗn hợp ban đầu ( biết thể tích các khí đang ở dktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
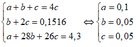
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%

Đáp án D
Đặt a, b, c lần lượt là số mol CH4, C2H4, C2H2 (trong 8,6 gam X)
Ta có: 16a + 28b + 26c = 8,6 (1)
b + 2c = 0,3 (2)
Mặt khác: Gọi số mol của CH4, C2H4, C2H2 trong 13,44 lít hỗn hợp X lần lượt là kx, ky, kz
![]() (3)
(3)
![]()
kc kc
Ta có
nkết tủa ![]() (4)
(4)
Lấy (3) chia (4) được
![]() (5)
(5)
Từ (1), (2) và (5) được

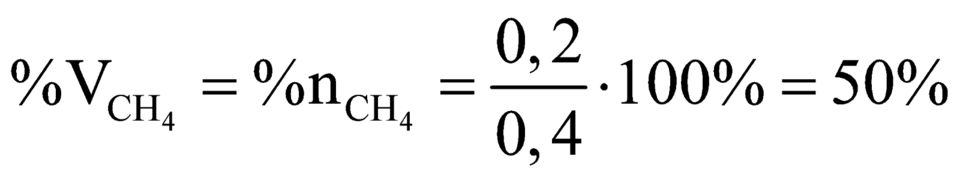

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c
=> 16a + 28b + 26c = 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b + 2c = 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
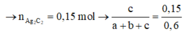
Giải hệ: a=0,2; b=0,1;c=0,1 nên %V CH4 =50%.

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c => 16a + 28b + 26c = 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b + 2c = 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
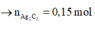
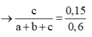
Giải hệ: a=0,2; b=0,1;c=0,1 nên %V CH4 =50%.

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c => 16a+28b+26c= 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b+2c= 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
→ n A g 2 C 2 = 0 , 15 m o l → c a + b + c = 0 , 15 0 , 6
Giải hệ: a=0,2; b=0,1; c=0,1 nên % V C H 4 =50%.

Gọi số mol của CH4 , C2H4 , C2H2 lần lượt là x , y , z
Ta có 16x + 28y + 26z = 8,6 (1)
t/d với Br: C2H4 + Br2 y--------> y
C2H2 + 2Br2
z --------> 2z => y + 2z = 0,3 (2) 0,6 mol X t/d AgNO3 trong NH3
C2H2 ------> C2Ag2
0,15 < ------ 0,15 Lập luận:
0,6 mol X t/d AgNO3 trong NH3 ----------> 0,15 mol kết tủa
8,6 g X ( tương ứng x + y + z mol ) t/ AgNO3 trong NH3 --------> z mol kết tủa ( n kết tủa = z)
=> 0,6 / ( x + y + z) = 0,15 /z <=> x + y - 3z = 0 (3) Từ (1) (2) (3) giải hệ => nCH4 = 0,3 => %CH4 = 50%
=> Đáp án A

a, Ta có: \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
\(16n_{CH_4}+28n_{C_2H_4}=3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,1\left(mol\right)\\n_{C_2H_4}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{3}.100\%\approx53,33\%\\\%m_{C_2H_4}\approx46,67\%\end{matrix}\right.\)
- Ở cùng điều kiện nhiệt độ và áp suất, % số mol cũng là %V.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,15}.100\%\approx66,67\%\\\%V_{C_2H_4}\approx33,33\%\end{matrix}\right.\)
b, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Có: m tăng = mC2H4 = 0,05.28 = 1,4 (g)
a) \(n_{hh}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a+b=0,15\\16a+28b=3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,15}.100\%=66,67\%\\\%V_{C_2H_4}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{3}.100\%=53,33\%\\\%m_{C_2H_4}=100\%-53,33\%=46,67\%\end{matrix}\right.\)
b) \(m=m_{C_2H_4}=0,05.28=1,4\left(g\right)\)

Ta có: \(n_{Br_2}=\dfrac{1,6}{160}=0,01\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,01\left(mol\right)\)
\(\Rightarrow\%V_{C_2H_4}=\dfrac{0,01.22,4}{0,5}.100\%=44,8\%\)
\(\Rightarrow\%V_{CH_4}=100-44,8=55,2\%\)