cho 28g hỗn hợp A gồm:axetilen,etilen,etan tác dụng hết AGNO3/NH3 thấy tạo thành 96g kết tủa vàng nhạt. Nếu cho hỗn hợp trên tác dụng với dd Br2 dư thì thấy tối đa 500ml Br2 2M a. Viết pt phản ứng xảy ra b.Tính khối lượng mỗi chất trong hỗn hợp A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$C_2H_2 + 2AgNO_3 + 2NH_3 \to Ag_2C_2 + 2NH_4NO_3$
Theo PTHH :
n C2H2 = n Ag2C2 = 48/240 = 0,2(mol)
$C_2H_4 + Br_2 \to C_2H_4Br_2$
$C_2H_2 + 2Br_2 \to C_2H_2Br_4$
n Br2 = 2n C2H2 + n C2H4 = 80/160 = 0,5(mol)
=> n C2H4 = 0,5 - 0,2.2 = 0,1(mol)
Vậy :
%V C2H2 = 0,2.22,4/8,96 .100% = 50%
%V C2H4 = 0,1.22,4/8,96 .100% = 25%
%V CH4 = 100% -50% - 25% = 25%

Đáp án A
Propen: CH2=CH-CH3, vinylaxetilen: CH≡C-CH=CH2.
Cho tác dụng với AgNO3/NH3 → Kết tủa: CAg≡C-CH=CH2 → n(↓) = 0,1 mol
→ n(C4H4) = 0,1 mol
Ta có: n(C3H6) + 2n(C4H4) = 0,35 → n(C3H6) = 0,35 – 0,1. 2 = 0,15 mol

Đáp án A
Propen: CH2=CH-CH3, vinylaxetilen: CH≡C-CH=CH2.
Cho tác dụng với AgNO3/NH3 → Kết tủa: CAg≡C-CH=CH2 → n(↓) = 0,1 mol
→ n C 4 H 4 = 0,1 mol
Ta có: n C 3 H 6 + 2 n C 4 H 4 = 0,35 → n C 3 H 6 = 0,35 – 0,1. 2 = 0,15 mol

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
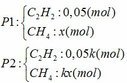
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 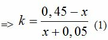
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
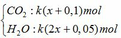
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
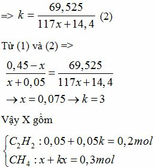
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam



\(n_{Br_2}=0,5.2=1\left(mol\right)\\ C_2H_2+2AgNO_3+2NH_3\rightarrow Ag_2C_2+2NH_4NO_3\\ n_{Ag_2C_2}=\dfrac{96}{240}=0,4\left(mol\right)\\ n_{C_2H_2}=n_{Ag_2C_2}=0,4\left(mol\right)\Rightarrow m_{C_2H_2}=0,4.26=10,4\left(g\right)\\ \Rightarrow m_{hh\left(C_2H_4,C_2H_6\right)}=28-10,4=17,6\left(g\right)\\ C_2H_2+2Br_2\rightarrow C_2H_2Br_4\left(1\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\left(2\right)\\ n_{Br_2\left(2\right)}=1-2.0,4=0,2\left(mol\right)\\ n_{C_2H_4}=n_{Br_2\left(2\right)}=0,2\left(mol\right)\\ m_{C_2H_4}=0,2.28=5,6\left(g\right)\\ m_{C_2H_6}=17,6-5,6=12\left(g\right)\\ hhA:\left\{{}\begin{matrix}C_2H_4:5,6\left(g\right)\\C_2H_6:12\left(g\right)\\C_2H_2:10,4\left(g\right)\end{matrix}\right.\)