khối lượng phân tử của hợp chất aluminium Sulfate được tạo bởi 2 nguyên tử Al và 3 nhóm nguyên tử
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Đặt:Al_a^{III}O_b^{II}\left(a,b:nguyên,dương\right)\\ QT.hoá.trị:a.III=II.b\Rightarrow\dfrac{a}{b}=\dfrac{II}{III}=\dfrac{2}{3}\Rightarrow a=2;b=3\\ CTTQ:Al_2O_3\\ m_{Al_2O_3}=2.27+3.16=102\left(đ.v.C\right)\)

Gọi công thức của A là H 3 X O y (vì nhóm X O y hóa trị III nên theo quy tắc hóa trị ta xác định được phân tử có 3 nguyên tử H)
Phân tử khối của H 2 S O 4 : 2 + 32 + 16.4 = 98 (đvC)
Vì A nặng bằng phân tử H 2 S O 4 nên PTK của A là 98 đvC
Theo đề bài, ta có khối lượng của nguyên tố oxi trong hợp chất là:
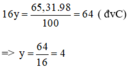
→ có 4 nguyên tử oxi trong hợp chất A.
Vậy nguyên tử khối của X là: 98 – (3 + 64) = 31 (đvC)

Hợp chất X : $R_2O_5$(lập CTHH dựa quy tắc hóa trị)
$M_X = 2R + 5O = 2R + 16.5 = 142\ đvC \Rightarrow R = 31(đvC)$
Vậy R là nguyên tố Photpho, CTHH X : $P_2O_5$
Hợp chất Y : $A_2(SO_4)_a$(lập CTHH dưa quy tắc hóa trị )
$M_Y = 2A + 96a =142 : 0,355 = 400\ đvC$
Với a = 1 thì A = 152 - loại
Với a = 2 thì A = 104 - loại
Với a = 3 thì A = 56 (Fe)
Vậy A là nguyên tố Fe, CTHH Y : $Fe_2(SO_4)_3$


\(PTK\left[Al_2\left(SO_4\right)_3\right]=27\cdot2+\left(32+16\cdot4\right)\cdot3=342\left(amu\right)\)
Al2(SO4)3