(2 điểm). Đốt cháy hoàn toàn 13 gam axetilen trong không khí
a. Tính khối lượng mỗi sản phẩm thu được
b. Tính thể tích không khí đã dùng? (biết rằng oxi chiếm 20% thể tích không khí).
c. Tính khối lượng muối thu được khi dẫn toàn bộ khí cacbonic qua dung dịch nước vôi trong dư ?

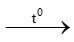 Fe3O4 (1)
Fe3O4 (1)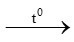 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
a, PT: \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{C_2H_2}=\dfrac{13}{26}=0,5\left(mol\right)\)
Theo PT: \(n_{CO_2}=n_{C_2H_2}=1\left(mol\right)\Rightarrow m_{CO_2}=1.44=44\left(g\right)\)
\(n_{H_2O}=n_{C_2H_2}=0,5\left(mol\right)\Rightarrow m_{H_2O}=0,5.18=9\left(g\right)\)
b, Theo PT: \(n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=1,25\left(mol\right)\Rightarrow V_{O_2}=1,25.22,4=28\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=140\left(l\right)\)
c, PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=1\left(mol\right)\Rightarrow m_{CaCO_3}=1.100=100\left(g\right)\)
n C2H2 = 1326=0,52613=0,5 (mol)
2C2H2 + 3O2 ��→to 4CO2 + 2H2O
0,5 --> 0,75 --> 1 --> 0,5
a. mCO2 = n.M = 1. 44 = 44 (gam)
mH2O = n.M = 0,5 . 18 = 9 (gam)
b. V(O2) = n.22,4 = 0,75 . 22,4 = 16,8 (lít)
Ta có Oxi chiếm 20% thể tích không khí
=> V (Không khí) = ��2.100%20%=16,8.10020=8420%VO2.100%=2016,8.100=84(lít)
c. CO2 + Ca(OH)2 →→CaCO3 + H2O
1 --> 1
m CaCO3 = n.M = 1.100 = 100 (gam)