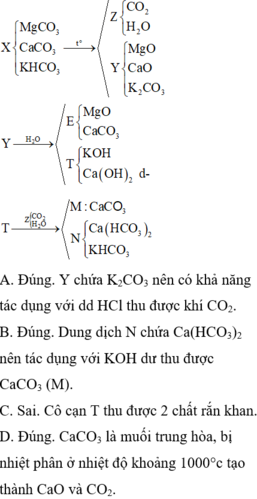
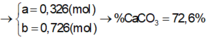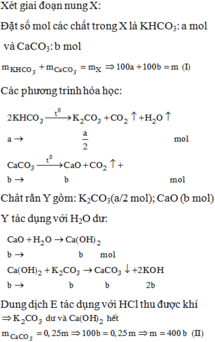3. Nung m gam hỗn hợp gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi thu được chất rắn X. Cho X vào lượng nước dư, sau phản ứng thu được chất rắn Y và dung dịch Z. Chia Z thành hai phần bằng nhau. Cho dung dịch Ca(HCO3)2 tới dư vào phần 1, sau phản ứng thu được 3 gam kết tủa. Cho từ từ dung dịch HCl 0,2M vào phần 2 đến khi không còn khí thoát ra thì thể tích dung dịch HCl đã dùng là 200 ml. Tìm giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho HCl vào Z thấy có khi thoát ra → Z gồm KOH và K2CO3.
Gọi: \(\left\{{}\begin{matrix}n_{KOH}=x\left(mol\right)\\n_{K_2CO_3}=y\left(mol\right)\end{matrix}\right.\) (trong 1/2Z)
- Cho pư với Ca(HCO3)2:
\(HCO_3^-+OH^-\rightarrow CO_3^{2-}\)
__________x________x (mol)
\(Ca^{2+}+CO_3^{2-}\rightarrow CaCO_3\)
________x+y________x+y (mol)
\(\Rightarrow x+y=\dfrac{3}{100}=0,03\left(mol\right)\left(1\right)\)
- Cho pư với HCl.
\(H^++OH^-\rightarrow H_2O\)
x______x (mol)
\(H^++CO_3^{2-}\rightarrow HCO_3^-\)
y_______y________y (mol)
\(H^++HCO_3^-\rightarrow CO_2+H_2O\)
y_________y (mol)
⇒ nH+ = x + 2y = 0,2.2 = 0,04 (mol) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,01\left(mol\right)\end{matrix}\right.\)
→ Z gồm: 0,04 (mol) KOH và 0,02 (mol) K2CO3
BTNT K, có: nKHCO3 = nKOH + 2nK2CO3 = 0,08 (mol)
BTNT OH: nCa(OH)2 = 1/2nKOH = 0,02 (mol)
BTNT Ca: nCaCO3 = nCaO = nCa(OH)2 = 0,02 (mol)
⇒ m = 0,08.100 + 0,02.100 = 10 (g)

Dung dịch E chứa $KOH$ và $K_2CO_3$
Bảo toàn C ta có: $n_{K_2CO_3/(pu)}=0,15(mol)$
Bảo toàn $H^+$ ta có: $n_{KOH/(pu)}=0,1(mol)$
Nhận thấy phản ứng tỉ lệ với nhau là $n_{K_2CO_3}:n_{KOH}=3:2$
Đặt: $n_{K_2CO_3/E}=3a;n_{KOH/E}=2a$
Bảo toàn $OH^-$ ta có: $n_{Ca(OH)_2}=n_{CaCO_3}=a(mol)$
Bảo toàn K ta có: $n_{KHCO_3}=8a(mol)$
$\Rightarrow a=0,1\Rightarrow m=m_{CaCO_3}=10(g)$

Do khi nhỏ HCl vào E thu được khí
=> Trong dd E chứa K2CO3
=> Ca2+ bị kết tủa hết
mZ = mCaCO3 = 0,25m (g)
=> \(n_{CaCO_3\left(Z\right)}=\dfrac{0,25m}{100}=0,0025m\left(mol\right)\)
Bảo toàn Ca: \(n_{CaCO_3\left(X\right)}=0,0025m\left(mol\right)\)
=> \(m_{KHCO_3}=m-100.0,0025m=0,75m\left(g\right)\)
=> \(n_{KHCO_3\left(X\right)}=\dfrac{0,75m}{100}=0,0075m\left(mol\right)\)
=> \(n_{K_2CO_3\left(Y\right)}=0,00375m\left(mol\right)\)
Bảo toàn C: \(n_{K_2CO_3\left(E\right)}=0,00375m-0,0025m=0,00125m\left(mol\right)\)
Bảo toàn K: \(n_{KOH}=2.0,00375m-2.0,00125m=0,005m\left(mol\right)\)
PTHH: KOH + HCl --> KCl + H2O
0,005m->0,005m
=> \(V_1=\dfrac{0,005m}{1}=0,005m\left(l\right)\)
K2CO3 + 2HCl --> 2KCl + CO2 + H2O
0,00125m->0,0025m
=> \(V_2=\dfrac{0,0025m+0,005m}{1}=0,0075m\left(l\right)\)
=> \(\dfrac{V_1}{V_2}=\dfrac{0,005m}{0,0075m}=\dfrac{2}{3}\)

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
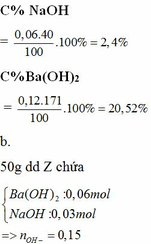
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g