Thổi 6,72 lít khí CO2 (đktc) vào cốc đựng 250 ml dung dịch KOH 2M (D = 1,2 g/ml) thu được dung dịch X.
1) Tính nồng độ phần trăm của dung dịch X.
2) Thêm lượng dư dung dịch bari clorua vào X, tính số gam kết tủa tạo ra.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Chọn đáp án D
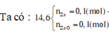


Có NH4NO3 vì nếu Y là N2 ![]()
Sau khi cho KOH vào thì K nó chạy đi đâu?Việc trả lời câu hỏi này sẽ giúp ta tiết kiệm rất nhiều thời gian và không cần quan tâm HNO3 thừa thiếu thế nào.
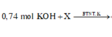

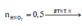
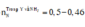
![]()
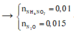
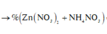
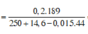
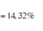

\(n_{KOH} = 0,5.1 = 0,5(mol)\\ n_{CO_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ n_{K_2CO_3} = a(mol) ; n_{KHCO_3} = b(mol)\\ 2KOH + CO_2 \to K_2CO_3 + H_2O\\ KOH + CO_2 \to KHCO_3\\ n_{KOH} = 2a + b = 0,5\\ n_{CO_2} = a + b = 0,3\\ \Rightarrow a = 0,2 ; b = 0,1\\ CaCl_2 + K_2CO_3 \to CaCO_3 + 2KCl\\ n_{CaCO_3} = n_{K_2CO_3} = 0,2(mol)\\ \Rightarrow m = 0,2.100 = 20(gam) \)
a)
$n_{CO_2} = 0,3(mol) ; n_{KOH} = 0,25.2 = 0,5(mol)$
Ta có :
$1< n_{KOH} : n_{CO_2} = 0,5 : 0,3 = 1,6<2$ Do đó, sản phẩm có $KHCO_3(a\ mol) ; K_2CO_3(b\ mol)$
$KOH + CO_2 \to KHCO_3$
$2KOH + CO_2 \to K_2CO_3 + H_2O$
Ta có :
$n_{KOH} = a + 2b = 0,5(mol)$
$n_{CO_2} = a + b = 0,3(mol)$
Suy ra: $a = 0,1 ; b = 0,2$
$m_{dd\ KOH} = D.V = 250.1,2 = 300(gam)$
$m_{dd\ X} = 300 + 0,3.44 = 313,2(gam)$
$C\%_{KHCO_3} = \dfrac{0,1.100}{313,2}.100\% =3,19\%$
$C\%_{K_2CO_3} = \dfrac{0,2.138}{313,2}.100\% = 8,81\%$
2)
$K_2CO_3 + BaCl_2 \to BaCO_3 + 2KCl$
$n_{BaCO_3} = n_{K_2CO_3} = 0,2(mol)$
$m_{BaCO_3} = 0,2.197 = 39,4(gam)$