Cho 8g lưu huỳnh trioxit vào nước thu được 250ml dung dịch axit sunfuric
a. Viết PTHH
b. Xác định nồng độ CM của axit thu đc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Số mol H2 = 0,1 mol
Phương trình phản ứng:
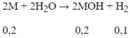
Tính được M = m : n = 7,8 : 0,2 = 39. Vậy kim loại cần tìm là K.
C M = 0 , 2 0 , 1 = 2 M

Số mol của đi photpho pentaoxxit
nP2O5 = \(\dfrac{m_{P2O5}}{M_{P2O5}}=\dfrac{28,4}{142}=0,2\left(mol\right)\)
a) Pt : P2O5 + 3H2O → 2H3PO4\(|\)
1 3 2
0,2 0,4
b) Số mol của axit photphoric
nH3PO4 = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của axit photphoric
mH3PO4 = nH3PO4. MH3PO4
= 0,4 . 98
= 39,2 (g)
Nồng độ phần trăm chất tan của axit photphoric
C0/0H3PO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{39,2.100}{28,4+150}=21,97\)0/0
Chúc bạn học tốt
a) PTHH: P2O5 + 3 H2O -> 2 H3PO4
nP2O5= 28,4/142=0,2(mol)
b) nH3PO4=2.0,2=0,4(mol)
=>mH3PO4=98. 0,4=39,2(g)
mddH3PO4=mP2O5+mH2O=28,4+150=178,4(g)
=>C%ddH3PO4=(39,2/178,4).100=21,973%

\(n_{H_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,6 1,2 0,6 0,6 ( mol )
\(m_{Fe}=0,6.56=33,6g\)
\(m_{FeCl_2}=0,6.127=76,2g\)
\(C_{M_{HCl}}=\dfrac{1,2}{0,6}=2M\)

`Fe + 2HCl -> FeCl_2 + H_2↑`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`n_[H_2] = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
`-> m_[Fe] = 0,3 . 56 = 16,8 (g)`
`-> m_[FeCl_2] = 0,3 . 127 = 38,1 (g)`
`b) C_[M_[HCl]] = [ 0,6 ] / [ 0,3 ] = 2 (M)`
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,3<---0,6<------0,3<-----0,3
=> \(\left\{{}\begin{matrix}m_{Fe}=0,3.56=16,8\left(g\right)\\m_{FeCl_2}=127.0,3=38,1\left(g\right)\\C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\end{matrix}\right.\)

gọi CTC của oxit là R2O3, đặt số mol R2O3 là 0.1(mol)
R2O3+6HCl-->2RCl3+3H2O
0.1 0.6 0.2 0.3 (mol)
C%ddHCl= 0.6x36.5x100/mdd=18.25
==>mddHCl=120(g)
C%ddspu=0.2x(R+35.5x3)x100/[0.1x(2R+48)+120]=23.897
==> R=56 : Fe
C% despite= 0,2x(R+35,5x3) x100/ [0.1x(2R+48)+120]=23.897.LLàm phiền bạn có thể giải thích cho mình rõ hơn chỗ phép tính này đk ko?
a) Pt: SO3 + H2O => H2SO4
b) nSO3 = \(\dfrac{8}{80}=0,1mol\)
Theo pt: nH2SO4 = nSO3 = 0,1 mol
=> CMH2SO4 = 0,1 : 0,25 = 0,4M
a)pthh SO3 + H2O --> H2SO4
0,1 0,1 mol
b) nSO3=8/80=0,1mol
CM H2SO4 = 0,1/0,25=0,4 M