2 bình chứa dung dịch acid sunfuric. Bình 1 chứa 4l dung dịch có nồng độ 70% và bình 2 chứa 3l dung dịch có nồng độ 90% ( cả 2 bình đều có dung dích 8l) . Hỏi phải đổ bao nhiêu lít dung dịch từ bình 2 sang bình 1 để có dung dịch acid nồng độ 80%, và ngược lại từ bình 1 sang bình 2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Phản ứng điện phân hai dung dịch:

Vì hai bình điện phân mắc nối tiếp nên cường độ dòng điện qua hai bình điện phân là như nhau.
Do đó số mol electron trao đổi ở hai bình điện phân bằng nhau.
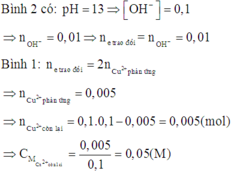

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
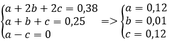
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%
bình \(1\) chứa số lít \(H_2SO4\) nguyên chất là : \(10.70\%=7l\)
gọi số lít từ bình \(2\) cần đổ sang là \(a\left(l\right)\)
có : sau khi đổ thì bình 1 có nồng độ \(H_2SO4\) là \(80\%\)
\(\Rightarrow\) \(\dfrac{7+0,9a}{10+a}=0,8\) \(\Leftrightarrow\) \(\left\{{}\begin{matrix}7+0,9a=0,8\left(10+a\right)\\7+0,9a=8+0,8a\\a=10\left(l\right)\end{matrix}\right.\) \(\Rightarrow\) \(a=10\) \(lít\)