đốt cháy hoàn toàn 11,2 lít khí metan trong không khí , sau đó sục toàn bộ sản phẩm thu được vào dd Ca(OH)2 dư thu được m gam chất rắn CaCO3 . Tính m biết phản ứng xảy ra khi sục CO2 vào dd Ca(OH)2 dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{NaOH}=2.0,03=0,06\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=2.0,02=0,04\left(mol\right)\)
\(n_{CaCO3}=\dfrac{3}{100}=0,03\left(mol\right)\)
Thứ tự các pthh :
\(C+O_2-t^o->CO_2\) (1)
\(CO_2+Ca\left(OH\right)_2-->CaCO_3+H_2O\) (2)
\(CO_2+2NaOH-->Na_2CO_3+H_2O\) (3)
\(CO_2+Na_2CO_3-->2NaHCO_3\) (4)
\(CO_2+CaCO_3-->Ca\left(HCO_3\right)_2\) (5)
Vì \(n_{CaCO3}< n_{Ca\left(OH\right)2}\left(0,03< 0,04\right)\) => Có 2 giá trị của CO2 thỏa mãn
TH1: CO2 thiếu ở pứ 2 => Chỉ xảy ra pứ (1) và (2) => Không có pứ hòa tan kết tủa
Theo pthh (2) : \(n_{CO_2}=n_{CaCO3}=0,03\left(mol\right)\)
Bảo toản C : \(n_C=n_{CO2}=0,03\left(mol\right)\)
=> m = 0,03.12 = 0,36 (g)
TH2 : CO2 dư ở pứ (2) ; (3); (4), đến pứ (5) thì thiếu => Có pứ hòa tan kết tủa
Xét pứ (2); (3); (4) ; (5) :
\(\Sigma n_{CO2}=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+n_{Na2CO3}+n_{CaCO3\left(tan\right)}\)
\(=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+\dfrac{1}{2}n_{NaOH}+\left(n_{CaCO3\left(sinh.ra\right)}-n_{CaCO3thu.duoc}\right)\)
\(=n_{Ca\left(OH\right)2}+n_{NaOH}+\left(n_{Ca\left(OH\right)2}-0,03\right)\)
\(=2n_{Ca\left(OH\right)2}+n_{NaOH}-0,03\)
\(=2.0,04+0,06-0,03\)
\(=0,09\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,09\left(mol\right)\)
\(\Rightarrow m=0,09.12=1,08\left(g\right)\)
Em làm đúng rồi đấy nhưng TH 2 bước cuối chắc tính nhầm kìa nCO2 = 0,11 mol , e sửa lại nhé.

\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CaCO_3}=n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\m_{CaCO_3}=0,1.100=10\left(g\right)\)

Câu 1/
\(2C\left(\dfrac{m}{12}\right)+O_2\left(\dfrac{m}{24}\right)\rightarrow2CO_2\left(\dfrac{m}{12}\right)\)
\(CO_2\left(\dfrac{m}{12}\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(\dfrac{m}{12}\right)+H_2O\)
Nếu như O2 thì tỷ khối của hỗn hợp so với O2 phải là: \(\dfrac{44}{32}=1,375>1,25\) vậy trong hỗn hợp khí phải có O2
\(n_C=\dfrac{m}{12}\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{V}{22,4}-\dfrac{m}{12}\left(mol\right)\)
\(\Rightarrow\dfrac{44.\dfrac{m}{12}+32.\left(\dfrac{V}{22,4}-\dfrac{m}{24}\right)}{\dfrac{m}{12}+\dfrac{V}{22,4}-\dfrac{m}{24}}=1,25.32=40\)
\(\Leftrightarrow15V-28m=0\left(1\right)\)
Ta lại có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(\Rightarrow\dfrac{m}{12}=0,06\Leftrightarrow m=0,72\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}15V-28m=0\\m=0,72\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m=0,72\left(g\right)\\V=1,344\left(l\right)\end{matrix}\right.\)

Đáp án B
Rắn X phải có A1 dư vì chỉ có A1 mới phản ứng với dung dịch NaOH tạo khí H2. Mặt khác do phản ứng hoàn toàn nên Fe3O4 hết.
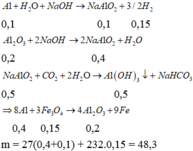

Đặt \(\left\{{}\begin{matrix}n_{CaCO_3}=x\\n_{MgCO_3}=y\end{matrix}\right.\) ( mol )
\(\Rightarrow m_{hh}=100x+84y=14,2\left(g\right)\) (1)
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\)
x x x ( mol )
\(MgCO_3\rightarrow\left(t^o\right)MgO+CO_2\)
y y y ( mol )
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,15 0,15 ( mol )
\(n_{CaCO_3}=\dfrac{15}{100}=0,15\left(mol\right)\)
\(\Rightarrow n_{CO_2}=x+y=0,15\left(mol\right)\) (2)
\(\left(1\right);\left(2\right)\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{0,1.100}{14,2}.100=70,42\%\\\%m_{MgCO_3}=100-70,42=29,58\%\end{matrix}\right.\)
\(m_{rắn}=m_{CaO}+m_{MgO}=0,1.56+0,05.40=7,6\left(g\right)\)
\(V_{CO_2}=0,15.22,4=3,36\left(l\right)\)

\(n_{C_2H_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ a,n_{O_2}=3.0,5=1,5\left(mol\right)\\ V_{O_2\left(đktc\right)}=1,5.22,4=33,6\left(l\right)\\ V_{kk\left(đktc\right)}=33,6.5=168\left(l\right)\\ b,n_{CO_2}=n_{H_2O}=2.0,5=1\left(mol\right)\\ m_{CO_2}=44.1=44\left(g\right);m_{H_2O}=18.1=18\left(g\right)\\ c,CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{Ca\left(OH\right)_2}=n_{CO_2}=1\left(mol\right)\\ m_{Ca\left(OH\right)_2}=1.74=74\left(g\right)\\ m_{ddCa\left(OH\right)_2}=\dfrac{74.100}{10}=740\left(g\right)\)

\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,2 0,4 0,2
CO2 + Ca(OH)2 ---> CaCO3 + H2O
0,2 0,2
\(\rightarrow\left\{{}\begin{matrix}x=0,2.100=20\left(g\right)\\V_{kk}=0,4.5.22,4=44,8\left(l\right)\end{matrix}\right.\)

a. \(n_{CO_2}=0,02\left(mol\right);n_{Ca\left(OH\right)_2}=0,008\left(mol\right)\Rightarrow n_{OH^-}=0,016\\ Tacó:\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,016}{0,02}=0,8\Rightarrow ChỉtạoCa\left(HCO_3\right)_2,CO_2dư\\ 2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2+H_2O\\ n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)_2}=0,016\left(mol\right)\\ \Rightarrow CM_{Ca\left(HCO_3\right)_2}=\dfrac{0,016}{0,4}=0,04M\)
\(b.n_{SO_2}=0,18\left(mol\right);n_{Ba\left(OH\right)_2}=0,2\left(mol\right)\Rightarrow n_{OH^-}=0,4\left(mol\right)\\Tacó:\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,4}{0,18}=2,22\Rightarrow Ba\left(OH\right) _2dư\\ SO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\\ n_{Ba\left(OH\right)_2dư}=0,2-0,18=0,02\left(mol\right)\\ \Rightarrow CM_{Ba\left(OH\right)_2dư}=\dfrac{0,02}{0,2}=0,1M\)

nCH4 = 11.2/22.4 = 0.5 (mol)
CH4 + 2O2 -to-> CO2 + 2H2O
0.5____________0.5
CO2 + Ca(OH)2 => CaCO3 + H2O
0.5_______________0.5
mCaCO3 = 0.5*100 = 50 (g)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 +2H_2O\\ CO_2 +C a(OH)_2 \to CaCO_3 + H_2O\\ n_{CaCO_3} = n_{CO_2} = n_{CH_4} = \dfrac{11,2}{22,4} = 0,5(mol)\\ m = 0,5.100 = 50(gam)\)