Để điều chế khí H2 trong phòng thí ngiệm,người ta cho 6,5g Zn vào dd H2SO4. a/ Viết pt phản ứng b/ Tính khối lượng H2SO4 đã dùng c/ Nếu dùng lượng H2 nói trên đi qua bột FeO nung núng thì khối lượng kim loại Fe thu đc là bào nhiêu???
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
a+b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,2\left(mol\right)\\n_{H_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,2\cdot160=32\left(g\right)\\V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
c) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,6\cdot65=39\left(g\right)\)
a,
nFe = 22,4/56 = 0,4 (mol)
PTHH
Fe2O3 + 3H2 ---to----) 2Fe + 3H2O (1)
theo phương trình (1) ,ta có:
nFe2O3 = 0,4 x 2 / 1 = 0,8 (mol)
mFe2O3 = 160 x 0,8 = 128 (g)
b,
theo pt (1)
nH2 = (0,4 x 3)/2 = 0,6 (mol)
=) VH2 = 0,6 x 22,4 = 13,44 (L)
c,
PTHH
Zn + H2SO4 -------------) ZnSO4 + H2 (2)
Số mol H2 cần dùng là 0,6 (mol)
Theo PT (2) :
nZn = nH2 ==) nZn = 0,6 x 65 = 39 (g)

9.
\(n_{ZnO}=\dfrac{16,2}{81}=0,2mol\)
\(ZnO+H_2\rightarrow\left(t^o\right)Zn+H_2O\)
0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
\(m_{Zn}=0,2.65=13g\)
10.
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
0,1 0,4 0,3 ( mol )
\(V_{H_2}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
\(Fe_3O_4+4CO\rightarrow\left(t^o\right)3Fe+4CO_2\)
0,1 0,4 0,3 ( mol )
\(V_{CO}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
nZnO = 16,2 : 81 = 0,2(mol)
pthh : ZnO + H2 -t--> Zn + H2O
0,2--->0,2-----> 0,2 (mol)
=> VH2 = 0,2 .22,4 = 4,48 (l)
=> mZn = 0,2 . 65 = 13 (g)
2
Fe3O4 + 4CO -t--> 3Fe + 4CO2
0,1-------> 0,4 -------->0,3 (mol)
Fe2O3 + 3H2 -t--> 2Fe + 3H2O
0,1------->0,3 -------->0,2 (mol)
=> VH2 = 0,3 .22,4 = 6,72(L)
=> VCO = 0,2 . 22,4 = 4,48 (L)
mFe= (0,3 + 0,2 ) . 56 = 28 (g)

a) 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b) \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
____\(\dfrac{4}{15}\)<----0,4<--------------------0,4
=> \(m_{Al}=\dfrac{4}{15}.27=7,2\left(g\right)\)
c) \(C_{M\left(H_2SO_4\right)}=\dfrac{0,4}{0,15}=2,667M\)

a, Ta có:
nZn = 13/65= 0,2(mol)
PTHH: Zn + H2SO4 → ZnSO4 + H2
0,2-----------------------------------0,2
Theo PT : nZnSO4 = 0,2.1/1 = 0,2(mol)
mZnSO4 = 0,2. 161 = 32,2(g)
b, Ta có:
Theo PT : nH2 = 0,2.1/1 = 0,2(mol)
VH2(đktc) = 0,2 . 22,4 = 4,48(l)
CuO+H2-to>Cu+H2O
0,2-----0,2
=>m Cu=0,2.64=12,8g
Cậu ơi cho tớ hỏi ngu tý là cái mà "0,2---------0,2" là ntn vậy ạ :"))?

a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
_____0,2____0,4___________0,2 (mol)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
c, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
____________0,2__2/15 (mol)
\(\Rightarrow m_{Fe}=\dfrac{2}{15}.56=\dfrac{112}{15}\left(g\right)\)
Số mol của 13 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
1 : 2 : 1 : 1 (g)
0,2\(\rightarrow\) 0,4 : 0,2 : 0,2 (mol)
a,Khối lượng của 0,4 mol HCl:
\(m_{HCl}=n.M=0,4.36,5=14,6\left(g\right)\)
b, Thể tích khí H2:
\(V_{H_2}=n.24,79=0,2.24,79=4,958\left(l\right)\)
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
Khối lượng của \(\dfrac{2}{15}\) mol Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{2}{\dfrac{15}{56}}\approx7,5\left(g\right)\)

2,24 lít hidro chứ chắc không phải 2,25 em hi?

Fe+H2SO4->FeSO4+H2
0,25--0,25-----0,25---0,25
CuO+H2-to>Cu+H2O
0,25----0,25
n Fe=0,25 mol
m H2SO4=0,25.98=24,5g
m H2=0,25.22,4=5,6l
m Cu=0,25.64=16g

cop tên ng ta nè
a) CuO+H2−to→Cu+H2OCuO+H2−to→Cu+H2O
nCuO(bđ)=1680=0,2(mol)nCuO(bđ)=1680=0,2(mol)
⇒nCuO(pứ)=0,2.80%=0,16(mol)⇒nCuO(pứ)=0,2.80%=0,16(mol)
nH2O=nCuO=0,16(mol)nH2O=nCuO=0,16(mol)
=> mH2O=0,16.18=2,88(g)mH2O=0,16.18=2,88(g)
b) nH2=0,15(mol)nH2=0,15(mol)
Lập tỉ lệ : 0,21>0,151⇒0,21>0,151⇒Sau phản ứng CuO dư
Chất rắn sau phản ứng là Cu, CuO dư
mcr=0,15.64+(0,2−0,15).80=13,6(g)mcr=0,15.64+(0,2−0,15).80=13,6(g)
c) Gọi x là số mol CuO phản ứng
mcr=(0,2−x).80+64x=13,28mcr=(0,2−x).80+64x=13,28
=> x=0,17 (mol)
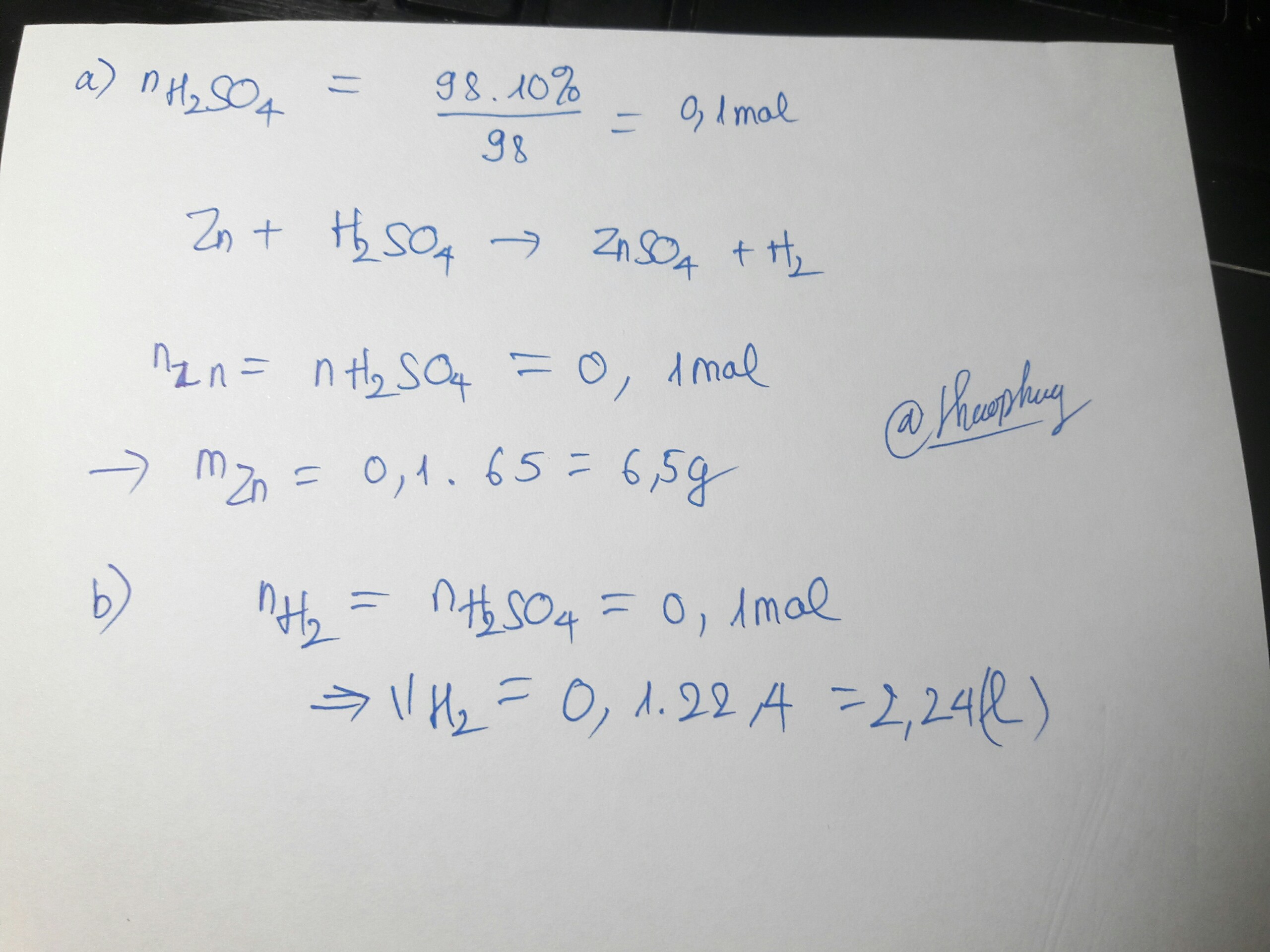
a.b.\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,1 0,1 0,1 ( mol )
\(m_{H_2SO_4}=0,1.98=9,8g\)
c.\(FeO+H_2\rightarrow\left(t^o\right)Fe+H_2O\)
0,1 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)