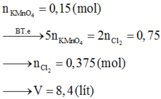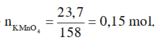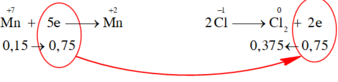cho 28,4 gam kmno4 phản ứng hết với dung dịch hcl đặc ( dư), thu được V lít khí cl2 (đktc). giá trị của V là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Số mol KMnO 4 là
![]()
Sơ đồ phản ứng:
K Mn + 7 O 4 ⏟ 0 , 3 mol + H Cl - 1 → Mn + 2 Cl 2 + Cl 2 ⏟ V lit 0 + KCl + H 2 O
Các quá trình nhường, nhận electron:
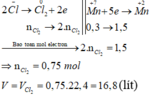

Đáp án B
![]() = 0,15(mol)
= 0,15(mol)
2KMnO4 + 16HCl → 5Cl2 + 8H2O + 2KCl + 2MnCl2
0,15 →0,375 (mol)
![]() = 0,375.22,4 = 8,4(l)
= 0,375.22,4 = 8,4(l)

Chọn đáp án B
n K M n O 4 = 23 , 7 158 = 0 , 15 ( m o l )
Bảo toàn electron 2 n C l 2 = 5 n K M n O 4 ⇒ n C l 2 = 0 , 375 m o l ⇒ V = 0 , 375 . 22 , 4 = 8 , 4 L

Đáp án C
![]() = 0,15 mol
= 0,15 mol
16HCl +2KMnO4 → 2KCl + 2MnCl2+ 5Cl2
0,15 → 0,375
Do H% = 60% => ![]() = 0,225 mol
= 0,225 mol
V = 0,225.22,4 = 5,04 (lít)

Chọn đáp án C
2 K M n O 4 + 16HCl → 2KCl + 2 M n C l 2 + 5 C l 2 + 8 H 2 O
n H C l = 14 , 6 36 , 5 = 0,4 (mol) => n C l 2 = 14 36 , 5 = 0,125 (mol)
=> V = 0,125.22,4 = 2,8 (lít)

- Theo bài ra \(\Rightarrow\left\{{}\begin{matrix}n_{KMnO_4}=0,1\\n_{KClO_3}=0,15\end{matrix}\right.\) ( mol )
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
.......0,1..........................................................0,25...........
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
....0,15................................0,45....................
\(\Rightarrow n_{HCl}=0,7\left(mol\right)\)
\(6KOH+3Cl_2\rightarrow KClO_3+5KCl+3H_2O\)
Ta có : \(m=m_{KOH}+m_{Cl_2}=139,3\left(g\right)\)
Vậy ...

\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{47,4}{158}=0,3mol\)
\(n_{KMnO_4}=\dfrac{0,3}{80\%}=0,375mol\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
2 16 2 2 5 8 ( mol )
0,375 > 2,5 ( mol )
0,375 0,9375 ( mol )
\(V_{Cl_2}=n_{Cl_2}.22,4=0,9375.22,4=21l\)
\(n_{KMnO_4\left(bd\right)}=\dfrac{47,4}{158}=0,3\left(mol\right)\) => \(n_{KMnO_4\left(pư\right)}=\dfrac{0,3.80}{100}=0,24\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,24------------------------------------->0,6
=> \(V=0,6.22,4=13,44\left(l\right)\)