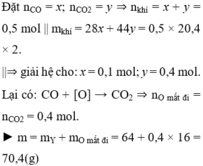Cho 3,24g hỗn hợp A dạng bột gồm Fe , FexOy vào ống sứ nung nóng rồi cho một luồng khí dư H2 đi chậm qua ống sứ để khử hoàn toànõi của oxit đó. Lượng nước được tạo thành có khối lượng là 0,81g chất rắn còn lại trong ống sứ có khối lượng 2,52g . xác định CT của oxit sắt và tính phần trăm theo khối luợng cuả sắt và oxit sắt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt nCO = x; nCO2 = y ⇒ nkhí = x + y = 0,5 mol || mkhí = 28x + 44y = 0,5 × 20,4 × 2.
⇒ giải hệ cho: x = 0,1 mol; y = 0,4 mol. Lại có: CO + [O] → CO2 ⇒ nO mất đi = nCO2 = 0,4 mol.
► m = mY + mO mất đi = 64 + 0,4 × 16 = 70,4(g)
Đáp án C

Đáp án C
Đặt nCO = x; nCO2 = y ⇒ nkhí = x + y = 0,5 mol || mkhí = 28x + 44y = 0,5 × 20,4 × 2.
||⇒ giải hệ cho: x = 0,1 mol; y = 0,4 mol. Lại có: CO + [O] → CO2 ⇒ nO mất đi = nCO2 = 0,4 mol.
► m = mY + mO mất đi = 64 + 0,4 × 16 = 70,4(g)

Giải thích: Đáp án A
TQ : CO + O -> CO2
Sau phản ứng thu được hỗn hợp khí (CO, CO2) => Oxit phản ứng hết
nCO + nCO2 = 0,5 mol
mCO + mCO2 = 2.20,4.0,5
=> nCO = 0,1 ; nCO2 = 0,4 mol = nO pứ
Bảo toàn khối lượng : m = mY + mO mất đi(pứ) = 70,4g

Đáp án D
Quy đổi A chỉ gồm Fe3O4 + CO → 19,2 gam (Fe : x mol + O : y mol) + CO2
19,2 gam (Fe : x mol + O : y mol) + HNO3 → Fe(NO3)3 + NO + H2O
Ta có hệ phương trình
(1) 56x + 16y = 19,2
(2) ĐLBT mol e : 3x = 2y + 0,1*3
→ x = 0,27 ; y = 0,255 → n(Fe3O4) = 0,09 mol → m1 = 20,880 gam
→ n(CO2) = n(CaCO3) = 0,09*4 – 0,255 = 0,105 → m2 = 20,685 gam
n(HNO3) = 0,27*3 + 0,1 = 0,91 mol