Tóm tắt và giải : Cầu 5. Dẫn 9 916 lít (đkc) hỗn hợp khi gồm etilen và metan tác dụng hoàn toàn với 250ml dung dịch brom . Khi phản ứng kết thúc thay khối lượng bình đựng nước brom tăng 7 gam. Tỉnh thành phần theo thể tích các khi trong hỗn hợp đầu bạ Tính nồng độ mol I dung dịch brom đã tham gia phản ứng C Tinh thể tích khi oxi (dke) cần dùng để đốt cháy hoàn toàn hỗn hợp khi trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


check lại giúp mình câu b) nhé
C2H2 + Br2 ra 1,2-đibrometen(tỉ lệ 1:1) hoặc 1,1,2,2-tetrabrometan(tỉ lệ 1:2) chứ không ra đibrometan nhé :v

\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(m_{tăng}=m_{Br_2}=m_{C_2H_2}=2,6g\)
\(\Rightarrow n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,1
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
0,1 0,25 0,2
\(\Rightarrow n_{CO_2\left(CH_4\right)}=0,4-0,2=0,2mol\)
\(\Rightarrow n_{CH_4}=0,2mol\Rightarrow n_{O_2}=0,4mol\)
a)\(\%V_{CH_4}=\dfrac{0,2}{0,4}\cdot100\%=50\%\)
\(\%V_{C_2H_2}=100\%-50\%=50\%\)
b)\(\Sigma n_{O_2}=0,4+0,25=0,65mol\)
\(\Rightarrow V_{O_2}=0,65\cdot22,4=14,56l\)
\(\Rightarrow V_{kk}=14,56\cdot5=72,8l\)

a.b.\(m_{tăng}=m_{C_2H_4}=2,8g\)
\(n_{C_2H_4}=\dfrac{2,8}{28}=0,1mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(n_{hh}=\dfrac{6,72}{22,4}=0,3mol\)
\(\rightarrow m_{CH_4}=\left(0,3-0,1\right).16=3,2g\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{2,8}{2,8+3,2}.100=46,67\%\\\%m_{CH_4}=100\%-46,67\%=53,33\%\end{matrix}\right.\)
c.\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,2 0,2 ( mol )
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
0,1 0,2 ( mol )
\(V_{CO_2}=\left(0,2+0,2\right).22,4=8,96l\)

a) nC2H4Br2=47/188=0,25(mol)
n(CH4,C2H4)=11,2/22,4=0,5(mol)
PTHH: C2H4 + Br2 -> C2H4Br2
0,25<----------0,25<---------0,25(mol)
mBr2(p.ứ)=0,25 x 160= 40(g)
b) V(C2H4,đktc)=0,25 x 22,4= 5,6(l)
=> %V(C2H4)=(5,6/11,2).100=50%
=>%V(CH4)=100% - 50%= 50%

\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow\left(t^o\right)CaCO_3+H_2O\)
0,8 0,8 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,5\\x+2y=0,8\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,5}.100=40\%\)
\(\%V_{C_2H_4}=100\%-40\%=60\%\)
\(m_{tăng}=m_{Ca\left(OH\right)_2}+m_{CaCO_3}=0,8.\left(74+100\right)=139,2g\)

Ta có: mC2H4 = m bình tăng = 2,8 (g)
\(\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{2,8}{4}.100\%=70\%\\\%m_{CH_4}=30\%\text{ }\end{matrix}\right.\)
Bạn tham khảo nhé!

Phương trình phản ứng:
C4H10⟶ CH4 + C3H6
C4H10⟶C2H4+C2H6
n a n k e n = n B r 2 = 25 , 6 160 = 0 , 16 ( m o l )
Gọi x là số mol butan còn dư. Số mol khí thoát ra khỏi bình bằng số mol butan ban đầu.
Khi đó: khối lượng khí đi ra khỏi bình là:
m = mbutan ban đầu - mkhí bị hấp thụ = 58.(x +0,16) - 5,32.
58 ( x + 0 , 16 ) - 5 , 32 x + 0 , 16 = 16 . 1 , 9625 ⇒ x = 0 , 04
⇒mbutan ban đầu = 58(l + x) = 11,6(g)
Đáp án D

a, PT: \(C_3H_6+Br_2\rightarrow C_3H_6Br_2\)
Ta có: m bình tăng = mC3H6 = 6,3 (g)
\(\Rightarrow n_{C_3H_6}=\dfrac{6,3}{42}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_3H_6}=\dfrac{0,15.22,4}{6,72}.100\%=50\%\\\%V_{C_2H_6}=100-50=50\%\end{matrix}\right.\)
b, Theo PT: \(n_{Br_2}=n_{C_3H_6}=0,15\left(mol\right)\Rightarrow C_{M_{Br_2}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
c, Theo PT: \(n_{C_3H_6Br_2}=n_{C_3H_6}=0,15\left(mol\right)\Rightarrow C_{M_{C_3H_6Br_2}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
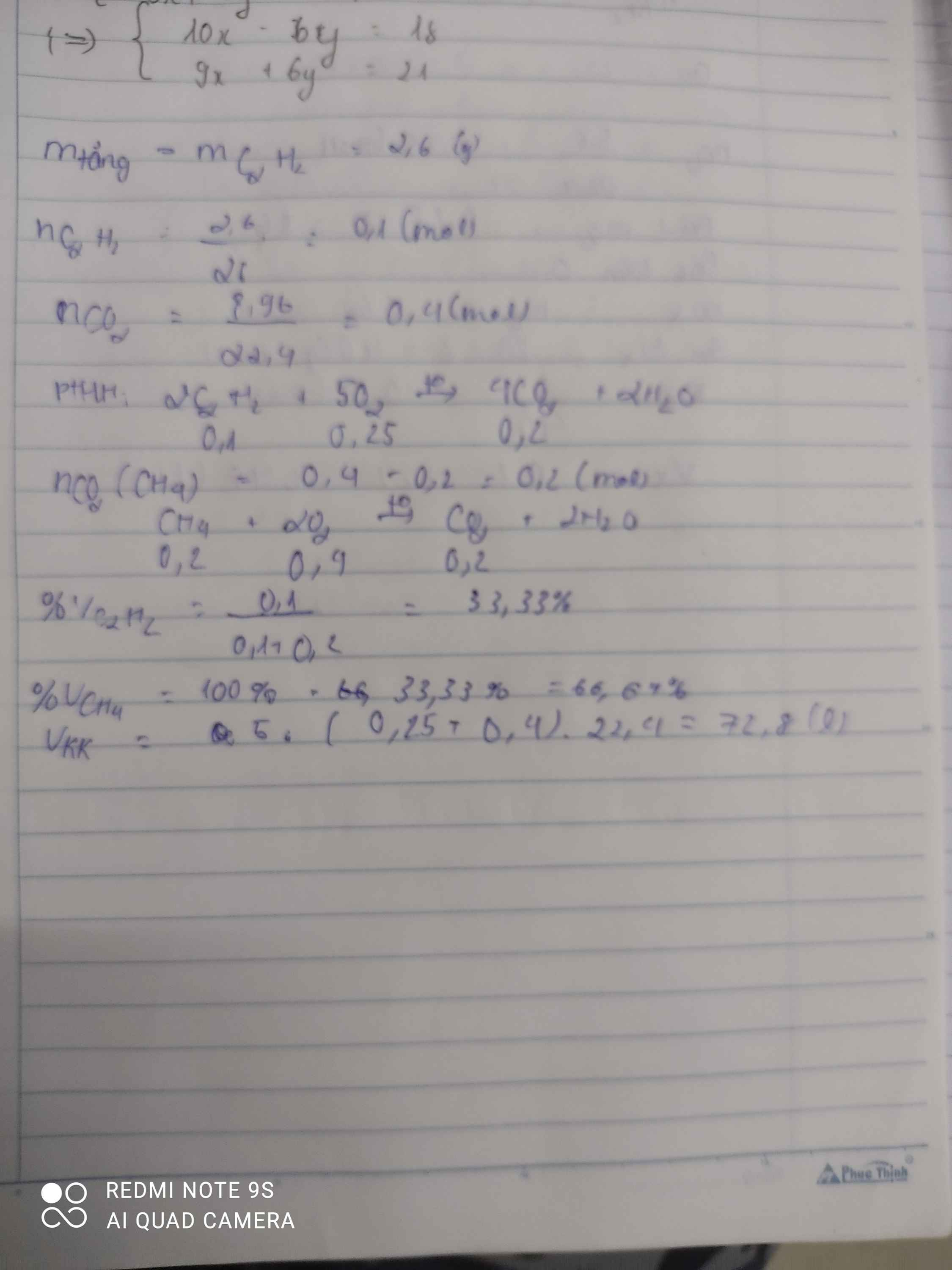
a) mtăng = mC2H4 = 7 (g)
=> \(n_{C_2H_4}=\dfrac{7}{28}=0,25\left(mol\right)\)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,25.24,79}{9,916}.100\%=62,5\%\\\%V_{CH_4}=100\%-62,5\%=37,5\%\end{matrix}\right.\)
b)
PTHH: C2H4 + Br2 ---> C2H4Br2
0,25-->0,25
=> \(C_{M\left(dd.Br_2\right)}=\dfrac{0,25}{0,25}=1M\)
c)
\(n_{CH_4}=\dfrac{9,916}{24,79}-0,25=0,15\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,15-->0,3
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,25-->0,75
=> VO2(đkc) = (0,3 + 0,75).24,79 = 26,0295 (l)