Câu 19: Trong phòng thí nghiệm có các kim loại Zn và Fe, các dung dịch axit H2SO4 loãng và HCl. Muốn điều chế được 2,24 lít khí H2 (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất?
A. Fe và H2SO4 B. Fe và HCl C. Zn và H2SO4 D. Zn và HCl
Câu 20: Khử 5,6g sắt(III) oxit bằng khí hiđro .Thể tích khí hiđro(đktc) cần dùng là:
A. 5,04 lít B. 6,72 lit C. 2,24 lít D. 3,36 lít
Câu 21: Số gam sắt cần tác dụng hết với axit clohiđric để cho 4,48 lít khí hiđro (đktc) là:
A. 11,2g B.28g C. 5,6g D. 3,7g



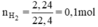
B D A