Cho 31,9gam hỗn hợp gồmNaX và NaY (X, Y là hai halogen ởhai chu kỳliên tiếp) vào dung dịch AgNO3dư thì thu được 57,4 gam kết tủa. a)Tính phần trăm khối lượng của mỗi muối trong hỗn hợp ban đầu.
b)Bằngphương pháp hóa học, hãy phân biệt 2 dung dịch riêng biệt của 2 muối trên.


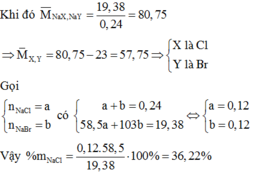

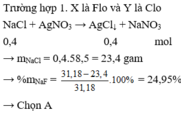


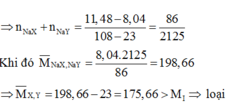


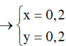
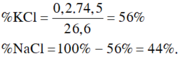
a) Giả sử MX < MY
TH1: Nếu trong hỗn hợp có NaF
=> muối còn lại là NaCl
\(n_{AgCl}=\dfrac{57,4}{143,5}=0,4\left(mol\right)\)
=> nNaCl = 0,4 (mol)
=> mNaCl = 0,4.58,5 = 23,4 (g)
\(\%m_{NaCl}=\dfrac{23,4}{31,9}.100\%=73,35\%\)
\(\%m_{NaF}=\dfrac{31,9-23,4}{31,9}.100\%=26,65\%\)
TH2: Nễu trong hh không có NaF
Gọi công thức chung của 2 muối là NaZ
\(n_{AgZ}=\dfrac{57,4}{108+M_Z}\left(mol\right)\)
=> \(n_{NaZ}=\dfrac{31,9}{23+M_Z}=\dfrac{57,4}{108+M_Z}\)
=> MZ = 83,333 (g/mol)
=> NaX, NaY lần lượt là NaBr, NaI
Gọi \(\left\{{}\begin{matrix}n_{NaBr}=a\left(mol\right)\\n_{NaI}=b\left(mol\right)\end{matrix}\right.\)
=> 103a + 150b = 31,9 (1)
\(\left\{{}\begin{matrix}n_{AgBr}=a\left(mol\right)\\n_{AgI}=b\left(mol\right)\end{matrix}\right.\)
=> 188a + 235b = 57,4 (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{131}{470}\left(mol\right)\\b=\dfrac{1}{47}\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{NaBr}=\dfrac{\dfrac{131}{470}.103}{31,9}.100\%=90\%\\\%m_{NaI}=\dfrac{\dfrac{1}{47}.150}{31,9}.100\%=10\%\end{matrix}\right.\)
b)
TH1: Nếu là NaF và NaCl
- Cho các dd tác dụng với dd AgNO3:
+ Không hiện tượng: NaF
+ Kết tủa trắng: NaCl
NaCl + AgNO3 --> NaNO3 + AgCl
TH2: Nếu là NaBr và NaI
- Cho các dd tác dụng với dd AgNO3:
+ Kết tủa vàng nhạt: NaBr
NaBr + AgNO3 --> AgBr + NaNO3
+ Kết tủa vàng: NaI
NaI + AgNO3 --> AgI + NaNO3