Viết PTHH phản ứng của Hiđro với các chất sau:oxi,sắt(II) oxit,sắt (III) oxit,oxit sắt từ bạc oxit và cho biết các phản ứng đó thuộc loại phản ứng gì? Mình thank you trước nhé
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Fe2O3 + 3H2 → 2Fe + 3H2O (phản ứng thế)
b) SO3 + H2O → H2SO4 (phản ứng hoá hợp)
c) 2Al + Fe2O3 → 2Fe + Al2O3 (phản ứng thế)
d) CaO + H2O → Ca(OH)2 (phản ứng hoá hợp)
e) 2K + 2H2O → 2KOH + H2 (phản ứng thế)
f) Zn + H2SO4 → ZnSO4 + H2 (phản ứng thế)

a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 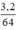 = 0,05 mol
= 0,05 mol
nFe = 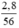 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 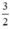 . nFe =
. nFe = 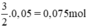 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\) - pư hóa hợp
b, \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\) - pư hóa hợp
c, \(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\) - pư thế
d, \(SO_3+H_2O\rightarrow H_2SO_4\) - pư hóa hợp
e, \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\) - pư oxi hóa khử
f, \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\) - pư họa hợp
g, \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\) - pư phân hủy
h, \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) - pư phân hủy
i, \(Fe+2HCl\rightarrow FeCl_2+H_2\) - pư thế
j, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) - pư thế

a. Fe + O2 -to> Fe3O4
Na + O2 -to> Na2O
S + O2 -to> SO2
CH4 + O2 -to> CO2 + H2O
K + O2 -to> K2O
Al + O2 -to> Al2O3
P + O2 -to> P2O5
N + O2 -to> NO2
C + O2 -to> CO2
b. FeO + H2 -to> Fe + H2O
Fe2O3 + H2 -to> Fe + H2O
PbO + H2 -to> Pb + H2O
Fe3O4 + H2 -to> Fe + H2O
O2 + H2 -to> H2O
CuO + H2 -to> Cu + H2O
c. KClO3 -to> KClO + O2
KMnO4 -to> K2MnO4 + MnO2 + O2
H2O -dpdd> H2 + O2
d. Al + HCl -> AlCl3 + H2
Fe + HCl -> FeCl2 + H2
Zn + HCl -> ZnCl2 + H2
Mg + HCl -> MgCl2 + H2
Al + H2SO4 -> Al2(SO4)3 + H2
Fe + H2SO4 -> FeSO4 + H2
Zn + H2SO4 -> ZnSO4 + H2
Mg + H2SO4 -> MgSO4 + H2
e. Na + H2O -> NaOH + H2
K + H2O -> KOH + H2
Ca + H2O -> Ca(OH)2 + H2
Ba + H2O -> Ba(OH)2 + H2
CaO + H2O -> Ca(OH)2
Na2O + H2O -> NạOH
K2O + H2O -> KOH
SO3 + H2O -> H2SO4
P2O5 + H2O -> H3PO4
CO2 + H2O -> H2CO3
N2O5 + H2O -> HNO3
SO2 + H2O -> H2SO3

Em chuyển sang môn Hoá em nha!
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\\ ZnO+H_2\rightarrow\left(t^o\right)Zn+H_2O\\ Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\\ Al_2O_3+H_2:Không.phản.ứng\)
-Hidro với Đồng (II) oxit là: Cuo+H2 ⇒ Cu+H2O
-Hidro với Kẽm oxit là:ZnO+H2 ⇒ Zn+H2O
-Hidro với Sắt từ oxit là:Fe3O4+4H2 ⇒ 3Fe+4H2O
Tham khảo ạ

a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)

a)\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b)\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(HgO+H_2\rightarrow Hg+H_2O\)
\(PbO+H_2\rightarrow Pb+H_2O\)
c)\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O\rightarrow H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

a.\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
b.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
\(HgO+H_2\rightarrow\left(t^o\right)Hg+H_2O\)
\(PbO+H_2\rightarrow\left(t^o\right)Pb+H_2O\)
c.\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O⇌H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
CH4 +2O2 -t--> CO2 + 2H2O
C+O2 -t-> CO2
S + O2 -t--> SO2
4Al + 2O2 -t--> 2Al2O3
3Fe + 2O2 -t--> Fe3O4
b)
Fe2O3 + 3H2 -t-> 2Fe + 3H2O
HgO + H2 -t--> Hg + H2O
PbO + H2 -t--> H2O + Pb
c) 2Na + 2H2O --> 2NaOH + H2
CaO + H2O ---> Ca(OH)2
Na2O + H2O --> 2NaOH
SO2 + H2O ---> H2SO3
P2O5 + 3H2O --> 2H3PO4

a) Fe2O3 + 3H2 → 2Fe + 3H2O.
b) HgO + H2 → Hg + H2O.
c) PbO + H2 → Pb + H2O.
\((1)2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ (2) FeO + H_2 \xrightarrow{t^o} Fe + H_2O\\ (3) Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ \)
(1) : phản ứng hóa hợp
(2) : Phản ứng oxi hóa
3 là phản ứng gi ạ