Câu 9: Cho 32 g sắt (III) oxit tác dụng với axit clohydric sinh ra muối sắt (III) clorua và nước. Tính khối lượng axit phản ứng, muối sinh ra và nước.
giúp mik với nha. Cảm ơn các bn :)))
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

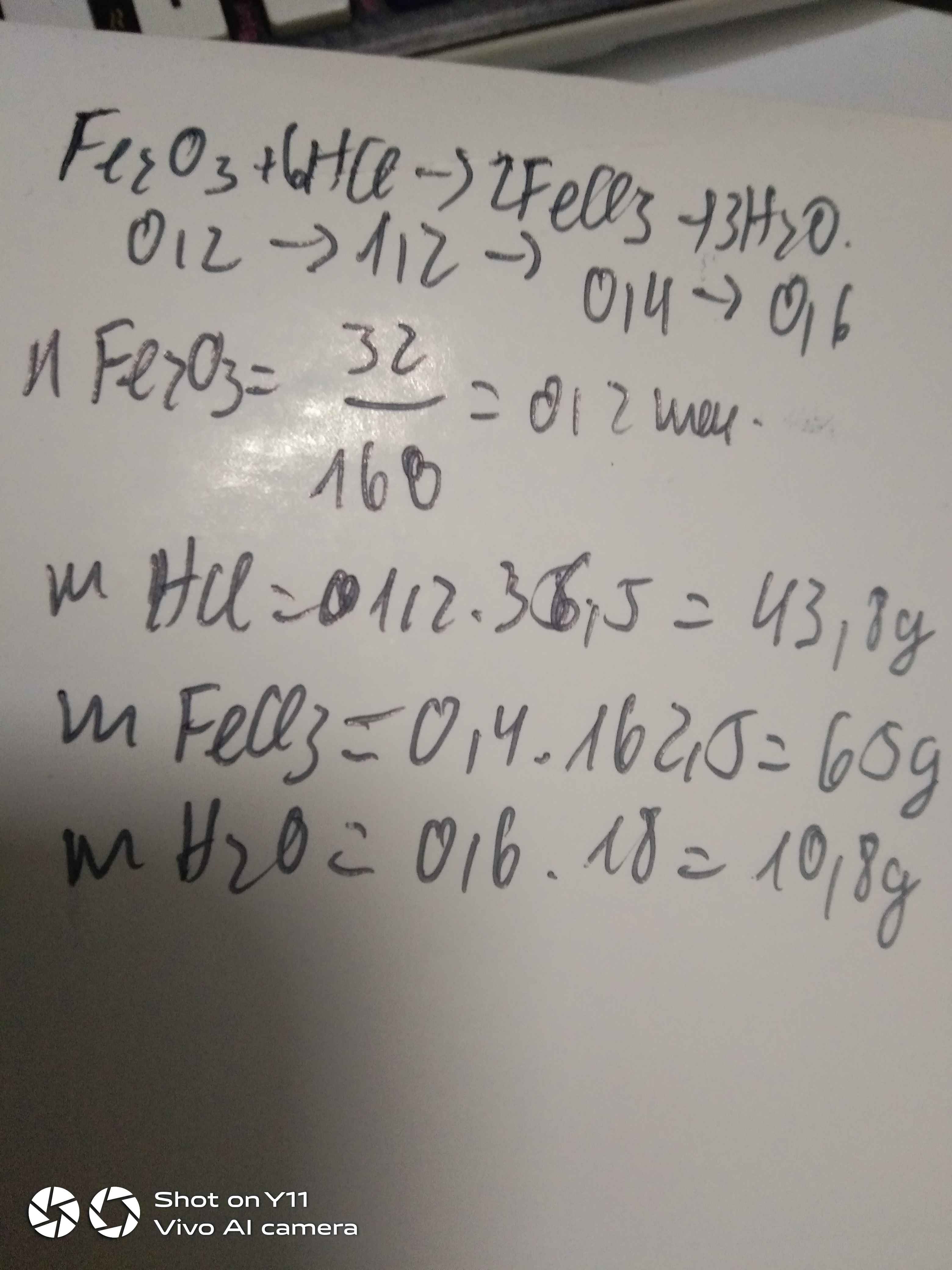
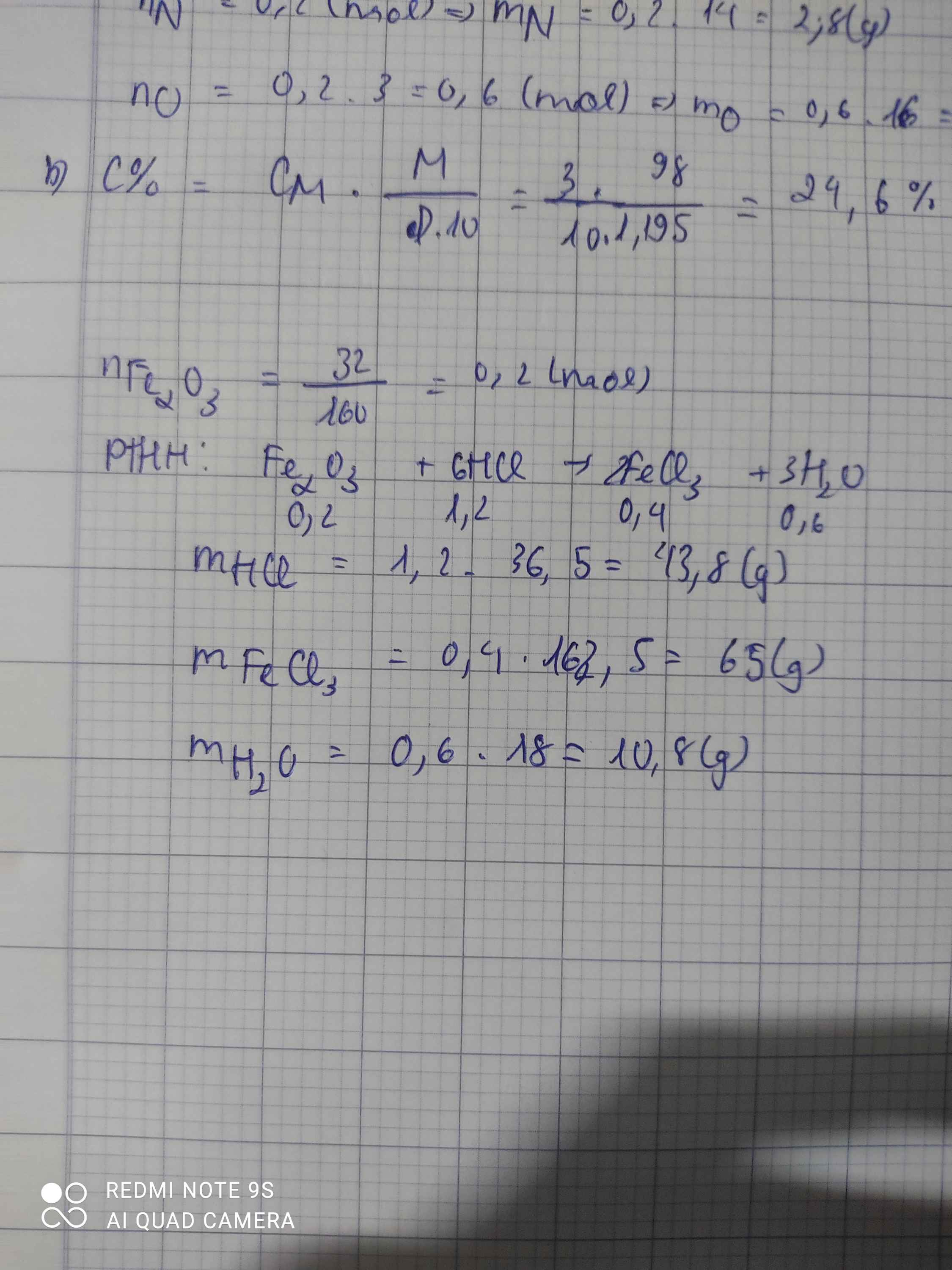

Câu 7 :
\(n_{H2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
\(\dfrac{8}{15}\) 0,8 \(\dfrac{4}{15}\) 0,8
\(n_{H2SO4}=\dfrac{0,8.3}{3}=0,8\left(mol\right)\)
⇒ \(m_{H2SO4}=0,8.98=78,4\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,8.1}{3}=\dfrac{4}{15}\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=\dfrac{4}{15}.342=91,2\left(g\right)\)
\(n_{Al}=\dfrac{0,8.2}{3}=\dfrac{8}{15}\left(mol\right)\)
⇒ \(m_{Al}=\dfrac{8}{15}.27=14,4\left(g\right)\)
Chúc bạn học tốt

Bài 1 :
a) Pt : 2Ba + O2 → (to) 2BaO
b) Pt : 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
c) Pt : ZnCl2 + 2NaOH → Zn(OH)2 + 2NaCl
d) Pt : Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Chúc bạn học tốt

$a) Fe + 2HCl \to FeCl_2 + H_2$
$b) n_{Fe} = \dfrac{5,6}{56} = 0,1(mol)$
Theo PTHH : $n_{HCl} = 2n_{Fe} = 0,1.2 = 0,2(mol)$
$m_{HCl} = 0,2.36,5 = 7,3(gam)$
$c) n_{H_2} = n_{Fe} = 0,1(mol)$
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
a: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b: \(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)=n_{FeCl_2}\)
\(\Leftrightarrow n_{HCl}=2\cdot0.1=0.2\left(mol\right)\)
\(m=0.2\cdot36.5=7.3\left(g\right)\)
c: \(V_{H_2}=0.1\cdot22.4=2.24\left(lít\right)\)

a,\(n_{Mg}=\dfrac{9,6}{24}=0,4\left(mol\right);n_{H_2SO_4}=1,5.0,2=0,3\left(mol\right)\)
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,3 0,3 0,3
Ta có: \(\dfrac{0,4}{1}>\dfrac{0,3}{1}\) ⇒ Mg dư, H2SO4 pứ hết
\(m_{MgSO_4}=0,3.120=36\left(g\right)\)
b,\(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{Fe_2O_3}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
PTHH: 3H2 + Fe2O3 → 2Fe + 3H2O
Mol: 0,04 0,08
Ta có: \(\dfrac{0,3}{3}>\dfrac{0,04}{1}\) ⇒ H2 dư, Fe2O3 pứ hết
\(\Rightarrow m_{Fe}=0,08.56=4,48\left(g\right)\)

a. \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b. \(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{28}{56}=0,5\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5-------1---------0,5-----0,5
Theo PTHH: \(\Rightarrow n_{H_2}=n_{Fe}=0,5\left(mol\right)\)
\(V_{H_2}=n_{H_2}.22,4=0,5.22,4=11,2\left(l\right)\)
c. \(H_2+CuO\rightarrow Cu+H_2O\)
0,5-------0,5-----0,5----0,5
\(\Rightarrow m_{Cu}=n_{Cu}.M_{Cu}=0,5.64=32\left(g\right)\)

B1 : nFe = 11,2 /56 = 0,2 (mol)
Fe+ 2HCl -- . FeCl2 + H2
mFeCl2 = 0,2.127 = 25,4 (g)
VH2 = 0,2 .22,4 = 4,48 (l)
mHCl = 0,4.36,5 = 14,6(g)
C%\(_{ddHCl}=\dfrac{ }{ }\)\(\dfrac{14,6.100}{280}=5,2\%\)
C2 :
2Al + 3H2SO4 -- > Al2(SO4)3 + 3H2
nH2 = 17,92/22,4 = 0,8 (mol)
mAl = (2/3.0,8 ) .27 = 14,4 (g)
mAl2(SO4)3 = (1/3 . 0,8 ) . 342 = 91,2 (g)
mH2SO4 = 0,8 . 98 = 78,4 (g)
\(C\%_{ddH_2SO_4}=\dfrac{78,4.100}{120}=65,33\%\)

Bài 1:
1) Fe + 2HCl --> FeCl2 + H2
2) \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
_____0,3--------------->0,3--->0,3
=> nH2 = 0,3.22,4 = 6,72(l)
3) mFeCl2 = 0,3.127=38,1(g)
Bài 2
1) 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
2) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
______0,2<----------------------------------0,3
=> mAl = 0,2.27 = 5,4(g)