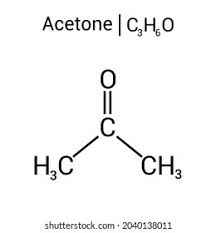
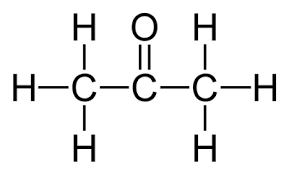
Đề bài : Đốt cháy hoàn toàn 6,3g 1 hợp chất hữu cơ X thu được 6,72 lít CO2(đktc) và 5,4g nước
a, Trong X có những nguyên tố hóa học nào ?
b, Xác định CTPT của X, biết tỉ khối X đối với oxi là 1,3125
c, CTCT có thể có của X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ ĐLBTKL:m_{tg}=m_{sp}=m_X+m_{O_2}=m_{CO_2}+m_{H_2O}=9+0,3.32=18,6\left(g\right)\\ n_{CO_2}:n_{H_2O}=1:1\Rightarrow n_{CO_2}=n_{H_2O}\\ Đặt:n_{CO_2}=n_{H_2O}=t\left(mol\right)\left(t>0\right)\\ \Rightarrow44t+18t=18,6\\ \Leftrightarrow t=0,3\left(mol\right)\\ \Rightarrow n_C=n_{CO_2}=0,3\left(mol\right);n_H=2.0,3=0,6\left(mol\right)\\ Trong.X:m_C=0,3.12=3,6\left(g\right);m_H=0,6.1=0,6\left(g\right)\\ Vì:m_C+m_H=3,6+0,6=4,2< 9\\ \Rightarrow X.chắc.chắn.có.O\\ \Rightarrow X.có:C,H,O\\ m_O=9-4,2=4,8\left(g\right)\\ n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
\(b,Đặt.CTĐGN:C_iH_dO_q\left(i,d,q:nguyên,dương\right)\\ Ta.có:i:d:q=0,3:0,6:0,3=1:2:1\\ \Rightarrow CTĐGN:CH_2O\\ c,Ta.có:9< d_{\dfrac{X}{He}}< 21\\ \Leftrightarrow9< \dfrac{M_X}{4}< 21\\ \Leftrightarrow36< M_X< 84\\ Đặt.CTTQ:\left(CH_2O\right)_a\left(a:nguyên,dương\right)\\ \Leftrightarrow36< 30a< 84\\ \Leftrightarrow1,2< a< 2,8\\ \Rightarrow a=2\\ \Rightarrow CTPT:C_2H_4O_2\)
Chúc em học tốt!

a, - Đốt X thu CO2 và H2O → X chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\Rightarrow n_H=0,4.2=0,8\left(mol\right)\)
⇒ mC + mH = 0,4.12 + 0,8.1 = 5,6 (g) < 12 (g)
→ X chứa C, H và O.
⇒ mO = 12 - 5,6 = 6,4 (g) \(\Rightarrow n_O=\dfrac{6,4}{16}=0,4\left(mol\right)\)
b, Gọi CTPT của X là CxHyOz.
⇒ x:y:z = 0,4:0,8:0,4 = 1:2:1
→ CTPT của X có dạng (CH2O)n
\(\Rightarrow n=\dfrac{60}{12+1.2+16}=2\)
Vậy: CTPT của X là C2H4O2.

\(n_{CO_2}=\dfrac{0.224}{22.4}=0.01\left(mol\right)\)
\(n_{H_2O}=\dfrac{0.27}{18}=0.015\left(mol\right)\)
\(n_O=\dfrac{0.23-0.01\cdot12-0.015\cdot2}{16}=0.005\left(mol\right)\)
\(\%C=\dfrac{0.01\cdot12}{0.23}\cdot100\%=52.17\%\)
\(\%H=\dfrac{0.015\cdot2}{0.23}\cdot100\%=13.04\%\)
\(\%O=100-52.17-13.04=34.79\%\)
\(n_C:n_H:n_O=0.01:0.03:0.005=2:6:1\)
CT đơn giản nhất : C2H6O
\(M_X=1.568\cdot29=46\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow46n=46\Rightarrow n=1\)
\(CT:C_2H_6O\)
nCO2= 0,01 (mol) -> nC=0,01(mol)
nH2O= 0,015(mol) -> nH=0,03(mol)
mX=mC+mH+mO
<=>0,23=0,1.12+0,03.1+mO
<=>mO=0,08
=>nO=0,005(mol)
Gọi CTTQ X: CxHyOz (x,y,z: nguyên, dương)
=>x:y:z=nC:nH:nO=0,01:0,03:0,005=2:6:1
=> CTĐGN C2H6O.
Mặt khác: M(X)= 1,568.29= 45,5 (thôi lấy tỉ khối 1,587 or 1,588 hợp lí hơn nha) (M(X) xấp xỉ 46 ~~~ )
=> (C2H6O)a=46
<=> 46a=46
<=>a=1
=>CTPT X : C2H6O

- Đốt X thu CO2 và H2O. → X chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,2.12 + 0,6.1 = 3 (g) < 4,6 (g)
→ X gồm: C, H và O.
mO = 4,6 - 3 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
- Gọi: CTHH của X là CxHyOz.
\(\Rightarrow x:y:z=0,2:0,6:0,1=2:6:1\)
→ CTĐGN của X là (C2H6O)n.
Mà: \(M_X=23.2=46\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{46}{12.2+6+16}=1\)
Vậy: CTHH của X là C2H6O.

a, - Đốt X thu CO2 và H2O.
→ X chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\Rightarrow n_H=0,4.2=0,8\left(mol\right)\)
⇒ mC + mH = 0,4.12 + 0,8.1 = 5,6 (g) < 12 (g)
→ X chứa C, H và O.
b, Ta có: mO = 12 - 5,6 = 6,4 (g) \(\Rightarrow n_O=\dfrac{6,4}{16}=0,4\left(mol\right)\)
Gọi CTPT của X là CxHyOz.
⇒ x:y:z = 0,4:0,8:0,4 = 1:2:1
→ CTPT của X có dạng (CH2O)n.
\(\Rightarrow n=\dfrac{60}{12+2.1+16}=2\)
Vậy: CTPT của X là C2H4O2.
c, CTCT: CH3COOH
PT: \(CH_3COOH+NaOH\underrightarrow{t^o}CH_3COONa+H_2O\)

Sửa đề: 5,04 gam -> 5,4 gam
a)
Theo ĐLBTNT: \(\left\{{}\begin{matrix}n_H=2n_{H_2O}=2.\dfrac{5,4}{18}=0,6\left(mol\right)\\n_C=n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\n_O=\dfrac{9-0,3.12-0,6}{16}=0,3\left(mol\right)\end{matrix}\right.\)
Vậy X chứa C, H, O
b) Đặt CTPT của X là CxHyOz
\(\Rightarrow n_X=\dfrac{9}{180}=0,05\left(mol\right)\Rightarrow\left\{{}\begin{matrix}x=\dfrac{0,3}{0,06}=6\\y=\dfrac{0,6}{0,05}=12\\z=\dfrac{0,3}{0,05}=6\end{matrix}\right.\)
Vậy X là C6H12O6

nCO2= 0,3(mol) -> nC=0,3(mol)
nH2O =0,25(mol) -> nH=0,5(mol)
mC+mH=0,3.12+0,5.1=4,1(g) < 5,7(g)
=>mO=5,7-4,1=1,6(g) -> nO=0,1(mol)
Gọi CTTQ X: CxHyOz (x,y,z: nguyên, dương)
Ta có: x:y:z= 0,3:0,5:1= 3:5:1
=> CT ĐG nhất X: C3H5O.
b) M(X)=57.2=114(g/mol)
Mà: M(X)=M(C3H5O)a= 57a
<=>114=57a
<=>a=2
=>CTPT X : C6H10O2
a,Giả sử hợp chất X bao gồm 2 nguyên tố là C và H
Ta có:nCO\(_2\)=\(\dfrac{6,72}{22,4}\)=0,3(mol)
\(\Rightarrow\)nC=nCO\(_2\)=0,3(mol)
Ta lại có :nH\(_2\)O=\(\dfrac{5,4}{18}\)=0,3(mol)
\(\Rightarrow\)nH=2nH\(_2\)O=0,6(mol)
Vì hợp chất X gồm hai nguyên tố C và H nên khối lượng của hai nguyên tố đó cũng chính là khối lượng của hợp chất X
\(\Rightarrow\)mX=mC+mH=12.0,3+2.0,6=4,8(g)<6,3(g)=mX(ban đầu)
\(\Rightarrow\)Hỗn hợp X gồm 3 nguyên tố C,H và O
b,Gọi CTHH của hợp chất X là CxHyOz
Bạn ơi đề lỗi r hợp chất X có khối lượng 6,4(g) ms đúng
Ta có:mO=6,4-4,8=1,6(g)\(\Leftrightarrow\)nO=\(\dfrac{1,6}{16}\)=0,1
Ta lại có:nC:nH:nO=x:y:z=0,3:0,6:0,1=3:6:1
\(\Rightarrow\)CTHH của hợp chất X là C3H6O
Gọi CTPT của hợp chất X là(C3H6O)a
Bạn ơi lại sai đề r tỉ khối của X với oxi là 1,8125
Ta có:dX/O\(_2\)=\(\dfrac{M_X}{32}\)=1,8125
\(\Leftrightarrow\)MX=32.1,8125=58
\(\Leftrightarrow\)(12.3+1.6+16)a=58
\(\Leftrightarrow\)a=1
⇒CTPT của hợp chất X là C3H6O
c,