Hòa tan hoàn toàn 2,44g hỗn hợp 3 kim loại Mg, Fe, Al bằng dd H2SO4 loãng thu được dd X. Cô cạn dd X được 11,08g muối khan. Tính thể tích H2 (đktc) sinh ra
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Gọi M là kim loại chung cho Mg, Fe và Al với hóa trị n
Gọi số mol H2 thu được là a mol
Sơ đồ phản ứng :
![]()
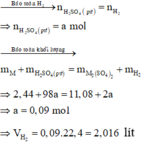

\(n_{H_2}=\dfrac{1,4874}{22,4}=0,06640178571\left(mol\right)\)
\(BTNT\) H:
\(2n_{H_2}=n_{HCl}\)
\(\Rightarrow n_{HCl}=\dfrac{7437}{56000}\left(mol\right)\)
BTKL có: \(m_{kl}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{muối}=1,58+\dfrac{7437}{56000}.36,5-2.0,06640178571=6,29\left(g\right)\)
bạn ơi tuy mình tự chỉnh đc nhma bạn có chú ý là điều kiện chuẩn ko ạ

\(5,41g\left\{{}\begin{matrix}Al\\Zn\end{matrix}\right.+HCl->\left\{{}\begin{matrix}AlCl3\\ZnCl2\end{matrix}\right.+H2\)
Ta có :
\(\left\{{}\begin{matrix}27x+65y=5,41\\133,5x+136y=17,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,08\\y=0,05\end{matrix}\right.\)
Bảo toàn e :
\(3x+2y=2.nH2\)
\(\Rightarrow nH2=0,17\left(mol\right)\)
\(\Rightarrow V=0,17.22,4=3,808\left(l\right)\)

\(\left\{{}\begin{matrix}Mg\\Zn\\Fe\end{matrix}\right.+H_2SO_4\rightarrow\left\{{}\begin{matrix}MgSO_4\\ZnSO_4\\FeSO_4\end{matrix}\right.+H_2\uparrow\)
\(m_{SO_4}=86,8-29=57,8\left(g\right)\)
\(\Rightarrow n_{H_2}=n_{H_2SO_4}=n_{SO_4}=0,6\left(mol\right)\)
\(\Rightarrow b=V_{H_2}=0,6.22,4=13,44\left(l\right)\)

Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
BTNT, có: \(n_{SO_4}=n_{H_2SO_4}=n_{H_2}=0,6\left(mol\right)\)
Mà: m muối = mKL + mSO4
⇒ m = mKL = 93,6 - 0,6.96 = 36 (g)
Bạn tham khảo nhé!

\(n_{H_2SO_4}=n_{H_2}=a(mol)\\ BTKL:\\ m_{hh}+m_{H_2SO_4}=m_{muối}+m_{H_2}\\ 29+98.a=86,6+2.a\\ \to a=0,6(mol)\\ V_{H_2}=0,6.22,4=13,44(l)\)

$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$
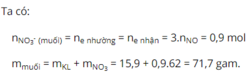
m_{tăng} = 11,08 - 2,44 = 96x
=> x = 0,09 (mol)
V = 2,016(l)
$m_{tăng}$