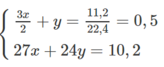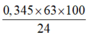Cho 6 gam mẫu hợp kim Al-Mg vào cốc chứa 100 gam dung dịch NaOH 16%, sau phản ứng thu được 6,72 lít khí ở điều khiện tiêu chuẩn.
a. Chứng tỏ rằng Al đã tham gia phản ứng hết.
b. Tính thành phần phần trăm về khối lượng của mẫu hợp kim và nồng độ phần trăm của chất tan trong dung dịch thu được sau phản ứng.
c. Nếu cho 9 gam mẫu hợp kim trên vào cốc chứa 200 gam dung dịch Hcl vừa đủ. Tính C% của dung dịch sau phản ứng?