Đốt cháy hoàn toàn V lít (đktc) hỗn hợp gồm C3H6, C3H4, C3H8 có tỉ khối so với H2 bằng 21,2 thu được 1,344 lít CO2 (đktc).Tìm V và khối lượng của nước tạo thành.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(C_3H_4+4O_2\underrightarrow{^{^{t^0}}}3CO_2+2H_2O\)
\(C_3H_6+\dfrac{9}{2}O_2\underrightarrow{^{^{t^0}}}3CO_2+3H_2O\)
\(C_3H_8+5O_2\underrightarrow{^{^{t^0}}}3CO_2+4H_2O\)
\(n_X=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(\Rightarrow n_{CO_2}=3\cdot n_X=3\cdot0.05=0.15\left(mol\right)\)
\(m_{CO_2}=0.15\cdot44=6.6\left(g\right)\)
\(m_X=21\cdot2\cdot0.05=2.1\left(g\right)\)
\(\Rightarrow m_H=m_X-m_C=2.1-0.15\cdot12=0.3\left(g\right)\)
\(n_H=0.3=0.3\left(mol\right)\)
\(\Rightarrow n_{H_2O}=0.15\left(mol\right)\)
\(m_{H_2O}=0.15\cdot18=2.7\left(g\right)\)
Gọi công thức hóa học chung của hỗn hợp X là \(C_3H_x\)
Có \(\overline{M_X}=21\cdot2=42đvC\Rightarrow12\cdot3+x\cdot1=42\)
\(\Rightarrow x=6\)
\(n_X=\dfrac{1,12}{22,4}=0,05mol\)
\(C_3H_6+\dfrac{9}{2}O_2\rightarrow3CO_2+3H_2O\)
0,05 0,15 0,15
\(m_{CO_2}=0,15\cdot44=6,6g\)
\(m_{H_2O}=0,15\cdot18=2,7g\)

Chọn A
Đề cho hỗn hợp X gồm 3 chất, nhưng chỉ có 2 giả thiết liên quan đến các chất đó nên quy đổi hỗn hợp X thành hỗn hợp gồm C 3 H 6 , C 3 H 8
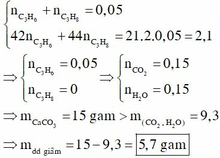

Em tham khảo bài này nhé!
https://hoc24.vn/cau-hoi/dot-chay-hoan-toan-159-gam-hon-hop-x-gomc3h4-c3h8-c3h6-co-ti-khoi-so-voi-hidro-la-212-a-viet-phuong-trinh-hoa-hoc-xay-ra-b-tinh-khoi-luong-co2-v.403660536930

\(n_X=\dfrac{0,896}{22,4}=0,08\left(mol\right)\)
\(M_X=21.2=42\left(g\text{/}mol\right)\\ \rightarrow m_X=0,08.42=3,36\left(g\right)\)
PTHH:
\(C_3H_4+4O_2\xrightarrow[]{t^o}3CO_2+H_2O\\ 2C_3H_6+9O_2\xrightarrow[]{t^o}6CO_2+6H_2O\\ C_3H_8+5O_2\xrightarrow[]{t^o}3CO_2+4H_2O\)
Theo PTHH: \(n_C=n_{CO_2}=3n_X=3.0,08=0,24\left(mol\right)\)
\(\rightarrow V_{CO_2}=0,24.22,4=5,376\left(l\right)\)
BTNT:
\(m_H=m_X=m_C=3,36-0,24.12=0,48\left(g\right)\\ \rightarrow n_H=\dfrac{0,48}{1}=0,48\left(mol\right)\)
Theo PTHH: \(n_{H_2O}=\dfrac{1}{2}n_H=\dfrac{1}{2}.0,48=0,24\left(mol\right)\)
\(\rightarrow m_{H_2O}=0,24.18=3,42\left(g\right)\)

Chọn C.
Đặt CTTQ của X là CxH4 Þ 12x + 4 = 28 Þ x = 2
Khi đốt cháy X thu được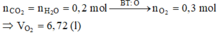

Câu 1 :
\(n_X=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(n_{CO_2}=\dfrac{12.32}{22.4}=0.55\left(mol\right)\)
\(\Rightarrow n_C=0.55\left(mol\right)\)
\(n_{H_2O}=\dfrac{10.8}{18}=0.6\left(mol\right)\)
\(\Rightarrow n_H=0.6\cdot2=1.2\left(mol\right)\)
\(m_X=m_C+m_H=0.55\cdot12+1.2=7.8\left(g\right)\)
\(\overline{M}_X=\dfrac{7.8}{0.15}=52\left(\dfrac{g}{mol}\right)\)
\(d_{\dfrac{X}{H_2}}=\dfrac{52}{2}=26\)
Câu 2 :
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Al}=\dfrac{a}{27}\left(mol\right)\)
\(n_{Fe}=\dfrac{a}{56}\left(mol\right)\)
Để cân thăng bằng thì lượng khí H2 thoát ra phải như nhau.
Vì :
\(n_{Fe}=\dfrac{a}{56}< n_{Al}=\dfrac{a}{27}\left(mol\right)\)
và lượng H2 sinh ra ở cả 2 phản ứng trên phụ thuộc vào HCl là như nhau
Để cân thăng bằng thì lượng HCl cho vào không vượt quá lượng tối đa để hòa tan Fe
\(n_{HCl}=2n_{Fe}=\dfrac{2a}{56}\left(mol\right)\)
\(\Rightarrow b\le\dfrac{2a}{56}\)
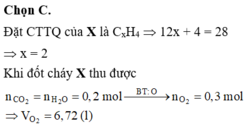

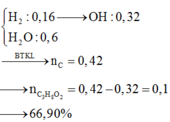
Quy đổi 2x mol C3H6 thành 1x mol C3H4 và 1x mol C3H8
\(\left\{{}\begin{matrix}n_{C_3H_4}=a\left(mol\right)\\n_{C_3H_8}=b\left(mol\right)\end{matrix}\right.\)
=> \(\dfrac{40a+44b}{a+b}=21,2.2=42,4=>a=\dfrac{2}{3}b\)
\(n_{CO_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Bảo toàn C: 3a + 3b = 0,06
=> a = 0,008(mol); b = 0,012 (mol)
=> V = (0,008+0,012).22,4 = 0,448(l)
Bảo toàn H: 2.nH2O = 4a + 8b
=> nH2O = 0,064
=> mH2O = 0,064.18 = 1,152(g)