Hòa tan 1,39g muối FeSO4.7H2O trong dung dịch H2SO4 loãng. Cho dung dịch này tác dụng với dung dịch KMnO4 0,1M. Tính thể tích dung dịch KMnO4 tham gia phản ứng.
( giúp anh mik đang ôn thi )
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học của phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
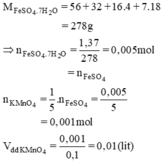

10FeSO4 + 2KMnO4 + 8H2SO4 -> 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
\(nFeSO4.7H2O=\dfrac{1.39}{56+32+64+7\times18}=5\times10^{-3}mol\) = nFeSO4
=> \(nKMnO4=5\times10^{-3}\times\dfrac{1}{5}=10^{-3}mol\)
=> VddKMnO4 = \(\dfrac{10^{-3}}{0.1}=0.01l\)

Đáp án C
nFeSO4 = nFeSO4.7H2O = 5,56: 278 = 0,02 mol
Fe+2 → Fe+3 + 1e
Mn+7 + 5e → Mn+2
=> Bảo toàn electron: nFeSO4 = 5nKMnO4 => nKMnO4 = 0,02: 5 = 0,004 mol
=> Vdd KMnO4 = 0,004: 0,1 = 0,04 lít = 40 ml

Đáp án C
Vì số mol của FeO bằng số mol của Fe2O3 nên ta coi hỗn hợp là Fe3O4
Ta có:
Fe3O4 +4H2SO4 → FeSO4 +Fe2(SO4)3 +4H2O
0,02 0,02
Trong 100 ml X sẽ có 0,01 mol FeSO4 nên:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
→ nKMnO4 = 0,02 mol → VKMnO4 = 0,02/0,1 = 0,2 l

Fe + H2SO4 → FeSO4 + H2
10FeSO4 + 2KMnO4 + 8H2SO4→ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
nFeSO4 = 5nKMnO4 = 0,3. 0,2. 5 = 0,3 mol
=> nFe = 0,3 mol <=> mFe = 0,3 .56= 16,8 gam
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
*tk
cái ảnh kia em nhìn quen quen nhỉ :))