khối lượng axit sunfuaric (H2SO4) có số phân tử bằng số phân tử có trong 11,2 lít khí hiđro H2 ở đktc là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Để số phân tử 2 chất bằng nhau thì số mol 2 chất cũng phải bằng nhau → từ đó tính khối lượng
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5(mol)\)
Ta có :\(n_{H_2SO_4}=n_{H_2}=0,5(mol)\)
\(-> m_{H_2SO_4}=0,5.98=49(g)\)
-> Chọn D

1mol H2SO4 có 6,022.1023 phân tử H2SO4
=> 7,3.1023 phân tử H2SO4 có số mol = \(\dfrac{7,3.10^{23}}{6,022.10^{23}}\)= 1,21 mol
<=> Khối lượng của 7,3.1023 phân tử H2SO4 = 1,21.98 = 118,58 gam
b) 8,8 gam CO2 có số mol = \(\dfrac{8,8}{44}\)=0,2 mol
=> V CO2 =0,2.22,4 = 4,48 lít
c) 6,72 lít O2 có số mol = 0,3 mol
Tương tự ta có 1 mol O2 thì có 6,022.1023 phân tử O2
=> 0,3 mol O2 thì có 0,3.6,022.123 = 1,806.1023 phân tử O2

Đáp án A
Xét hỗn hợp ankan Y ta có mY = 19,2 gam và nY = nX = 0,5 mol.
+ Đặt nC/Y = a và nH/Y = b ta có hệ || 12a + b = 19,2 Và b/2 – a = 0,5.
Giải hệ ⇒ nC = 1,3 mol và nH = 3,6 mol.
⇒ Số CTrung bình = 1,3/0,5 = 2,6 ⇒ Loại C và D.
⇒ Số HTrung bình = 4 ⇒ Loại B

\(n_{H_2}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
=> \(n_{H_2SO_4}=0,5\left(mol\right)\)
=> \(m_{H_2SO_4}=0,5.98=49\left(g\right)\)
=> D

a) \(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
b) \(n_{N_2}=\dfrac{1,8.10^{23}}{6.10^{23}}=0,3\left(mol\right)\)
=> \(m_{N_2}=0,3.28=8,4\left(g\right)\)
c) \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=>V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
d) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
=> Số phân tử H2 = 0,15.6.1023 = 0,9.1023
e) \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
f) \(n_{Cl_2}=\dfrac{3,6.10^{23}}{6.10^{23}}=0,6\left(mol\right)\)
=> VCl2 = 0,6.22,4 = 13,44(l)
g) \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> mO2 = 0,3.32 = 9,6(g)
h) \(n_{K_2O}=\dfrac{18,8}{94}=0,2\left(mol\right)\)
=> Số phân tử K2O = 0,2.6.1023 = 1,2.1023
i) \(n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
=> Số phân tử CaO = 0,2.6.1023 = 1,2.1023
nHCl = 0,2.1,5 = 0,3 (mol)
=> mHCl = 0,3.36,5 = 10,95(g)

a) Gọi số mol N2, O2 trong 6,72l khí A lần lượt là a, b
=> \(\left\{{}\begin{matrix}28a+32b=8,8\\a+b=\dfrac{6,72}{22,4}=0,3\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%V_{O_2}=\dfrac{0,1}{0,3}.100\%=33,33\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{N_2}=\dfrac{28.0,2}{8,8}.100\%=63,64\%\\\%m_{O_2}=\dfrac{32.0,1}{8,8}.100\%=36,36\%\end{matrix}\right.\)
b)
\(n_A=0,3\left(mol\right)\)
\(\Rightarrow n_{CO_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{CO_2}=0,3.44=13,2\left(g\right)\)
c) 2,2g A có thể tích là 1,68 lít
=> \(V_{H_2}=1,68\left(l\right)\)

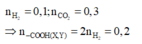
Căn cứ vào 4 đáp án ta có hỗn hợp X, Y (hỗn hợp A) gồm 1 axit đơn chức và 1 axit 2 chức.
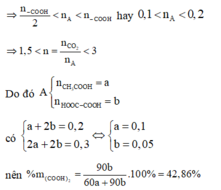
Đáp án A
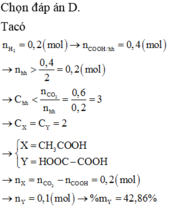
\(nH_2=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(N_{H_2}=0,5\text{×}6\text{×}10^{23}=3\text{×}10^{23}\)
Mà số phân tử của H2SO4 = H2
\(\text{⇒}N_{H_2}SO_4=\dfrac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\)
\(\text{⇒}mH_2SO_4=0,5\text{×}98=49\left(gam\right)\)