Câu 9: Dẫn V lít khí CO vào ống sứ chứa 4,8 g Fe2O3 nung nóng. Phản ứng xong, thu được chất rắn là kim loại sắt
và khí X có tỉ khối so với H2 bằng 20. Dẫn toàn bộ hỗn hợp khí này vào dung dịch Ca(OH)2 dư thu được m (g) kết
tủa.Viết PTPU và tìm V, m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi oxit kim loại phải tìm là MO và nCuO = a và nMO =2a
nHNO3 = 0.15 mol
Vì hiđro chỉ khử được những oxit kim loại đứng sau nhôm trong dãy điện hóa nên có 2 trường hợp xảy ra.
∙ Trường hợp 1: M đứng sau nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
MO + H2 → M + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3M + 8HNO3 → 3M(NO3)2 + 2NO + 4H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 16a/3 = 0.15 }
a = 0,01875 và M = 40 → M là Ca.
Trường hợp này loại vì CaO không bị khử bởi khí H2.
∙ Trường hợp 2: M đứng trước nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
MO + 2HNO3 → M(NO3)2 + 2H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 4a = 0.15 }
a = 0,0225 và M = 24 → M là Mg → Đáp án C

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
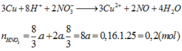
=>a=0,025=>80a+(M+16).2a=4,8
=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
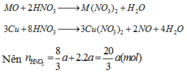
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
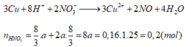
=>a=0,025=>80a+(M+16).2a=4,8=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
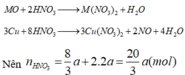
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24





$n_{Fe_2O_3} = \dfrac{4,8}{160} = 0,03(mol)$
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2$
$n_{CO_2} = 3n_{Fe_2O_3} = 0,09(mol)$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,09(mol)$
$m = 0,09.100 = 9(gam)$
Gọi $n_{CO} = a(mol)$
$M_{khí} = 20.2 = 40(g/mol)$
Ta có : $28a + 0,09.44 = (a + 0,09).40$
Suy ra : a = 0,03
Suy ra : $V = (0,09 + 0,03).22,4 = 2,688(lít)$