Cho 3,6 gam magie trên vào dung dịch chứa 14,6 gam axit clohidric (HCl) a. Hỏi sau phản ứng chất nào còn dư, dư bao nhiêu gam? b. Tính thể tích H2 (đktc)?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1.
a, \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,15 0,3
b, Ta có: \(\dfrac{0,15}{1}< \dfrac{0,5}{2}\) ⇒ Mg pứ hết, HCl dư
\(m_{HCldư}=\left(0,5-0,3\right).36,5=7,3\left(g\right)\)
c, \(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
2.
a, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 ---to→ 2P2O5
Mol: 0,2 0,25 0,1
b, \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c, \(m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(V_{kk}=5,6.5=28\left(l\right)\)

1.
nAl=\(\dfrac{5,4}{27}\)=0,2 mol
mHCl=\(\dfrac{175.14,6}{100}\)=25,55g
nHCl=\(\dfrac{25,55}{36,5}\)=0,7
2Al + 6HCl → 2AlCl3 + 3H2↑
n trước pứ 0,2 0,7
n pứ 0,2 →0,6 → 0,2 → 0,3 mol
n sau pứ hết dư 0,1
Sau pứ HCl dư.
mHCl (dư)= 36,5.0,1=3,65g
mcác chất sau pư= 5,4 +175 - 0,3.2= 179,8g
mAlCl3= 133,5.0,2=26,7g
C%ddHCl (dư)= \(\dfrac{3,65.100}{179,8}=2,03%\)%
C%ddAlCl3 = \(\dfrac{26,7.100}{179,8}\)= 14,85%
2.
200ml= 0,2l
mMg= \(\dfrac{4,2}{24}=0,175mol\)
Mg + 2HCl → MgCl2 + H2↑
0,175→ 0,35 → 0,175→0,175 mol
a) VH2= 0,175.22,4=3,92l.
b)C%dHCl= \(\dfrac{0,35}{0,2}=1,75\)M

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

\(n_{H_2}=\dfrac{17.92}{22.4}=0.8\left(mol\right)\)
\(n_{Fe_3O_4}=\dfrac{69.6}{232}=0.3\left(mol\right)\)
\(Fe_3O_4+4H_2\underrightarrow{t^0}3Fe+4H_2O\)
\(0.2..............0.8\)
\(m_{Fe_3O_4\left(dư\right)}=\left(0.3-0.2\right)\cdot232=23.2\left(g\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.8......................................0.8\)
\(m_{Zn}=0.8\cdot65=52\left(g\right)\)

Số mol của kẽm
nZn = \(\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,3 0,4 0,2 0,2
a) Lập tỉ số só sánh : \(\dfrac{0,3}{1}>\dfrac{0,4}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
Số mol dư của kẽm
ndư = nban đầu - nmol
= 0,3 - (\(\dfrac{0,4.1}{2}\))
= 0,1 (mol)
Khối lượng dư của kẽm
mdư = ndư . MZn
= 0,1 . 65
= 6,5 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mznCl2 = nZnCl2 . MZnCl2
= 0,2. 136
= 27,2 (g)
c) 4H2 + Fe3O4 → (to) 3Fe + 4H2O\(|\)
4 1 3 4
0,2 0,15
Số mol của sắt
nFe = \(\dfrac{0,2.3}{4}=0,15\left(mol\right)\)
Khối lượng của sắt
mFe = nFe. MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right);n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,6}{2}\Rightarrow Zn.dư\\ n_{H_2}=n_{Zn\left(p.ứ\right)}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ b,n_{Zn\left(dư\right)}=0,4-0,3=0,1\left(mol\right)\Rightarrow m_{Zn\left(dư\right)}=0,1.65=6,5\left(g\right)\)
`n_(Zn)=m/M=(26)/65=0,4(mol)`
`n_(HCl)=m/M=(21,9)/36,5=0,6(mol)`
`PTHH:Zn+2HCl->ZnCl_2 +H_2`
tỉ lệ: 1 ; 2 : 1 : 1
n(mol) 0,3<----0,6---->0,3----->0,3
\(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\left(\dfrac{0,4}{1}>\dfrac{0,6}{2}\right)\)
`=>` `Zn` dư, `HCl` hết, tính theo `HCl`
`V_(H_2)=n*22,4=0,3*22,4=6,72(l)`
`n_(Zn(dư))=0,4-0,3=0,1(mol)`
`m_(Zn(dư))=n*M=0,1*65=6,5(g)`

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)
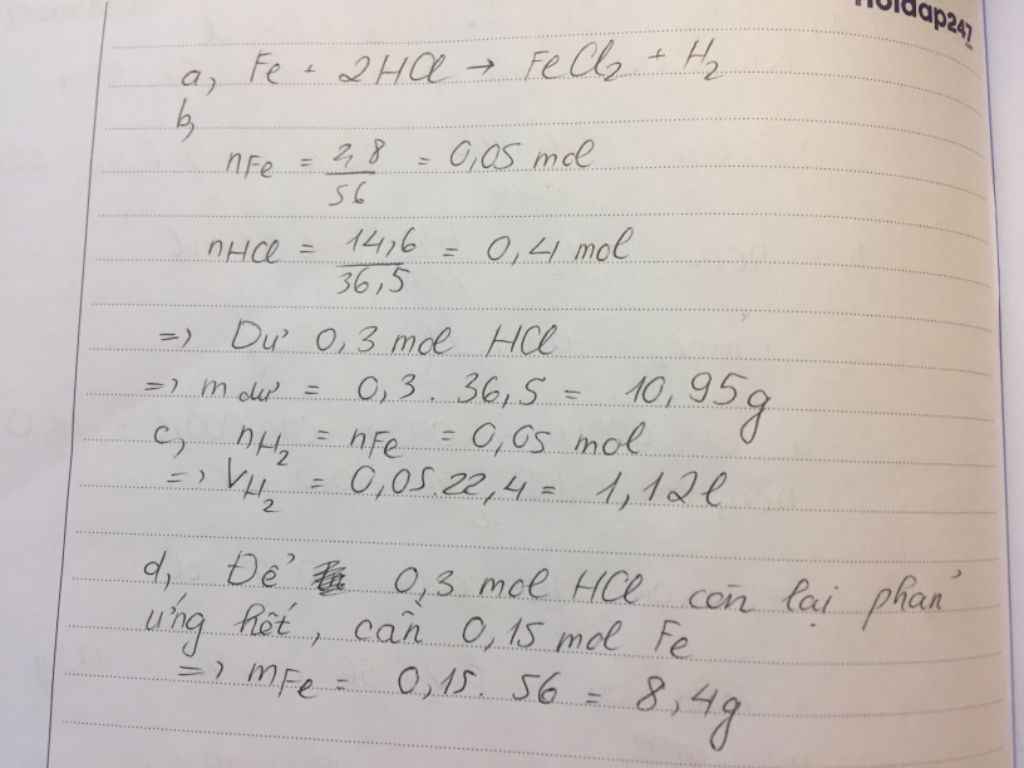
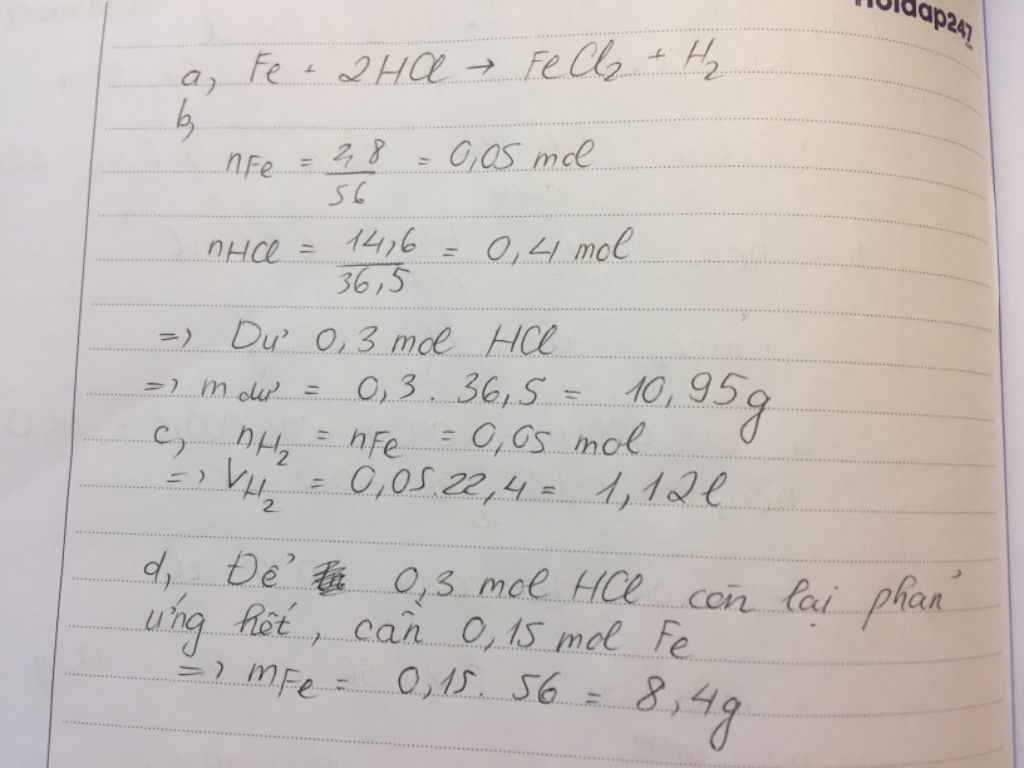
Theo gt ta có: $n_{Mg}=0,15(mol);n_{HCl}=0,4(mol)$
$Mg+2HCl\rightarrow MgCl_2+H_2$
Do đó sau phản ứng thì HCl dư 0,1(mol)
PTHH: Mg + 2HCl → MgCl2 + H2
b. nMg = 3,6 : 24 = 0,15 (mol)
nHCl = 14,6 : 36,5 = 0,4 (mol)
Tỉ lệ: nMg/1<nHCl/2 ⇒ Mg hết, HCl dư
m HCl = 0,4 . 14,6 (g)
Vậy ....