Em hãy cho biết tính chất hóa học của nhôm mỗi tính chất viết hai phường trình minh họa
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



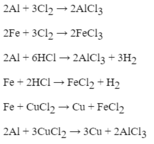

Bài giảng học thử
Video không hỗ trỡ trên thiết bị của bạn!
Bài 4. Chất béo (P1) - Hóa học lớp 9 - cô Hương Giang
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 2. Các oxit của cacbon (P2) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 9. Tính theo phương trình hóa học (tiết 2 - P1) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Chuyên đề 4. Bazơ (P1) - Ôn luyện Hóa học lớp 9 - cô Trịnh Mỹ Hạnh
Video không hỗ trỡ trên thiết bị của bạn!
Bài 1. Tính chất của kim loại (P1) - Hóa học lớp 9 - cô Hương Giang

b. Tính chất hóa học của nước
- Tác dụng với kim loại: nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
PTHH: K + H2O → KOH + H2
- Tác dụng với mốt sô oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
- Dung dịch bazơ làm quỳ tím chuyển xanh
VD: K2O + H2O → 2KOH
- Tác dụng với oxit axit như SO3, P2O5,… tạo thành axit tương ứng H2SO4, H3PO4,…
- Dung dịch axit làm quỳ tím chuyển đỏ
VD: SO3 + H2O → H2SO4
-Tác dụng với một số oxit axit tạo thành axit
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
-Tác dụng với một số oxit bazơ tạo hành bazơ
\(Na_2O+H_2O\rightarrow2NaOH\)
-Tác dụng với một số kim loại ở nhiệt độ thường tạo thành bazơ và khí H2
\(2K+2H_2O\rightarrow2KOH+H_2\)

Tham khảo :
1. Tác dụng với phi kim
a) Tác dụng với oxi
Al bền trong không khí ở nhiệt độ thường do có lớp màng oxit Al2O3 rất mỏng bảo vệ.
b) Tác dụng với phi kim khác
2. Tác dụng với axit
+ Axit không có tính oxi hóa: dung dịch axit HCl, H2SO4 loãng
2Al + 6HCl → 2AlCl3 + 3H2↑
+ Axit có tính oxi hóa mạnh: dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng.
Nhôm bị thụ động hoá trong dung dịch HNO3 đặc, nguội hoặc H2SO4 đặc nguội.
3. Tác dụng với oxit kim loại( Phản ứng nhiệt nhôm)
Lưu ý: Nhôm chỉ khử oxit của các kim loại đứng sau nhôm
4. Tác dụng với nước
- Phá bỏ lớp oxit trên bề mặt Al (hoặc tạo thành hỗn hống Al-Hg thì Al sẽ phản ứng với nước ở nhiệt độ thường)
2Al + 6H2O → 2Al(OH)3↓ + 3H2↑
5. Tác dụng với dung dịch kiềm
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
6. Tác dụng với dung dịch muối
- Al đẩy được kim loại đứng sau ra khỏi dung dịch muối của chúng:

- Tác dụng với kim loại:
Nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Ca, Ba, K,…
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
- Tác dụng với một số oxit bazo như CaO, K2O,… tạo ra bazo tương ứng Ca(OH)2, KOH,…
\(K_2O+H_2O\rightarrow2KOH\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
- Tác dụng với oxit axit như SO3, P2O5… tạo thành axit tương ứng H2SO4, H3PO4,…
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

Mình nghĩ cái này thuộc kiến thức cơ bản, bạn nên tự học trong SGK thì hơn là đi đăng câu hỏi ở Hoc24
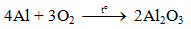
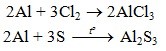
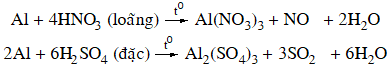
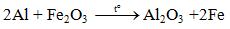
okay đợi xíu
Nhôm tác dụng với phi kim:
+) Nhôm tác dụng với oxi
PTHH : 4Al + 3O2 --nt---> 2Al2O3
+) Nhôm tác dụng với phi kim khác
PTHH: 2Al + 3S --nt---> Al2S3
Nhôm tác dụng với dd axit ( HCl, H2SO4 )
PTHH : 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 ↑
Nhôm tác dụng với dd muối
PTHH : 2Al + 3CuSO4 ----> Al2(SO4)3 + 3Cu
Nhôm tác dụng với dd kiềm
PTHH : 2Al + 2NaOH + 2H2O ----> 2NaAlO2 + 3H2 ↑