Nung nóng 31,6 g KMnO4. Tính thể tích Oxi thu được (đktc) nếu hiệu suất 80%. Tính thể tích Oxi thu được ở trên đem đốt 3,1g P. Tính khối lượng chất còn dư sau phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
a) Ta có: \(n_{KMnO_4}=\dfrac{94,8}{158}=0,6\left(mol\right)\)
\(\Rightarrow n_{O_2\left(lýthuyết\right)}=0,3\left(mol\right)\) \(\Rightarrow n_{O_2\left(thực\right)}=0,3\cdot90\%=0,27\left(mol\right)\)
\(\Rightarrow V_{O_2\left(thực\right)}=0,27\cdot22,4=6,048\left(l\right)\)
b) PTHH: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PTHH: \(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=0,18\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,18\cdot102=18,36\left(g\right)\)

\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,4}{5}\Rightarrow O_2dư\)
\(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=\dfrac{5}{4}.0,2=0,25\left(mol\right)\\ n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(n_{P_2O_5\left(lt\right)}=\dfrac{1}{2}n_P=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2\left(g\right)\\ m_{P_2O_5\left(tt\right)}=0,1.142.80\%=11,36\left(g\right)\)

PT: \(2KMnO_4+16HCl\rightarrow2MnCl_2+2KCl+5Cl_2+8H_2O\)
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
\(m_{HCl}=\dfrac{60.36,5}{100}=21,9\left(g\right)\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,6}{16}\), ta được KMnO4 dư.
Theo PT: \(n_{Cl_2\left(LT\right)}=\dfrac{5}{16}n_{HCl}=0,1875\left(mol\right)\)
Mà: H% = 80%
\(\Rightarrow n_{Cl_2\left(TT\right)}=0,1875.80\%=0,15\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
Bạn tham khảo nhé!

a.\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{31,6}{158}=0,2mol\)
\(PTHH:2KMnO_4\underrightarrow{np}K_2MnO_4+MnO_2+O_2\)
2 1 1 1 ( mol )
0,2 0,1
\(V_{O_2}=n.22,4=0,1.22,4=2,24l\)
b.\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
3 2 1 ( mol )
0,2 0,1
0,1 0,1 0,05 ( mol )
\(m_{Fe_3O_4}=n.M=0,05.232=11,6g\)

\(n_{KMnO_4}=\dfrac{15.8}{158}=0.1\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(n_{O_2}=\dfrac{0.1}{2}=0.05\left(mol\right)\)
\(V_{O_2}=0.05\cdot22.4=1.12\left(l\right)\)
\(b.\)
\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)
\(4.........5\)
\(0.2........0.05\)
\(LTL:\dfrac{0.2}{4}>\dfrac{0.05}{5}\Rightarrow Pdư\)
\(m_{P\left(dư\right)}=\left(0.2-0.04\right)\cdot31=4.96\left(g\right)\)
PTHH:2KMnO4--- K2MnO4+MnO2 +O2
ADCT nKmno4=15,8/158=0,1 mol
a, theo pt có nO2/nKmno4= 1/2
nO2=0,05 mol
ADCT V=n*22,4
VO2=0,05*22,4 =1,12 l
b, PTHH: 5O2+4P---2P2O5
ADCTnP=6,2/31=0,2 mol
Theo pt
nO2/5=0,01 bé hơn nP/4=0,05
P dư
theo pt nP(pư)/nO2=4/5
nP(p/ư)=0,04 mol
nP(dư)=0,05-0,04 =0,01 mol
ADCT:m=n*M
mP(dư)=0,01*31=0,31g

\(n_{KMnO_4}=\dfrac{63,2}{158}=0,4\left(mol\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,4 0,2
=> \(V_{O_2\left(lt\right)}=0,2.22,4=4,48\left(l\right)\\
V_{O_2\left(tt\right)}=\dfrac{90.4,48}{100}=4,032\left(l\right)\)
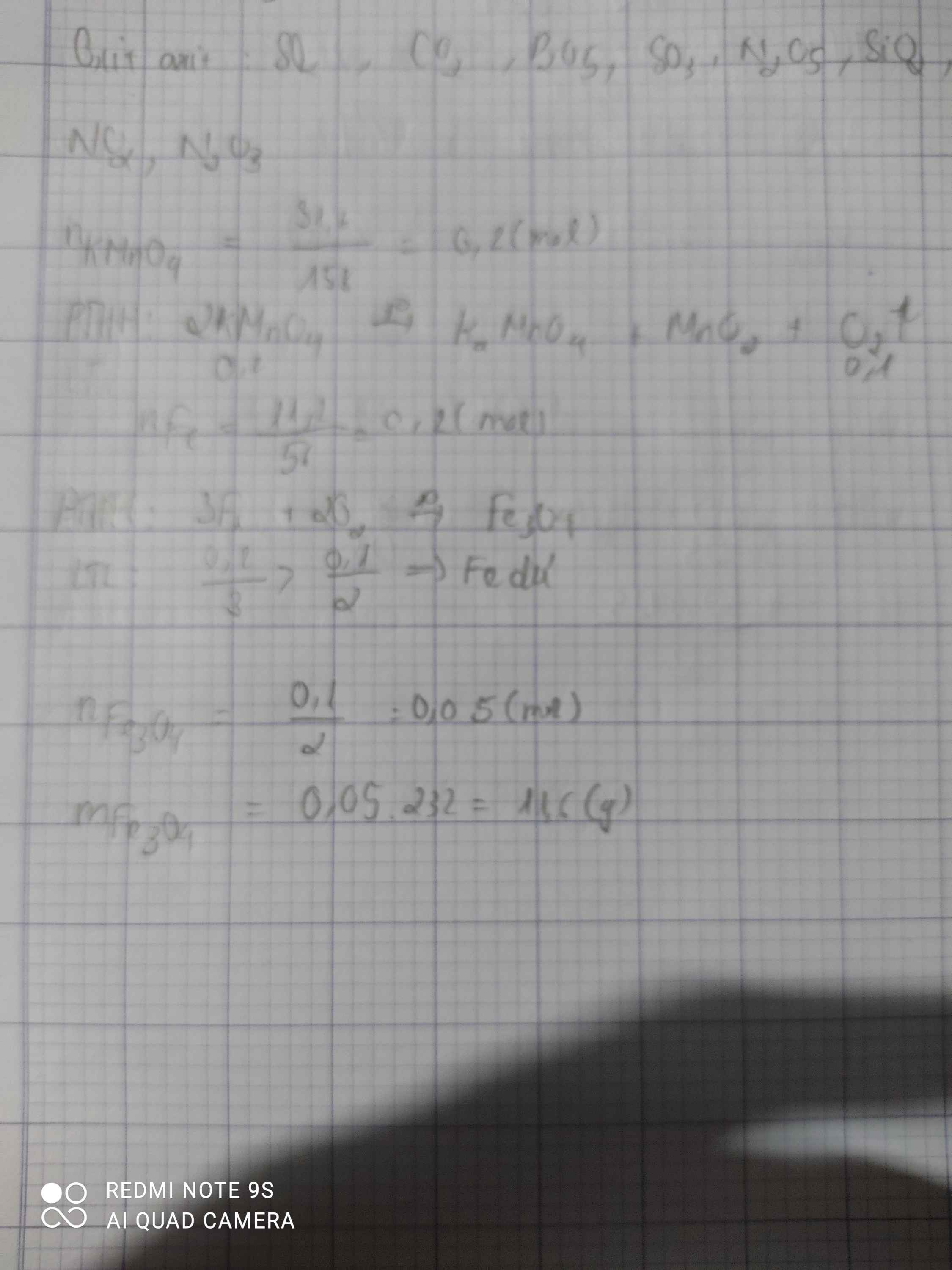

PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
Theo PT: \(n_{O_2\left(LT\right)}=\dfrac{1}{2}n_{KMnO_4}=0,1\left(mol\right)\)
Mà: H% = 80%
\(\Rightarrow n_{O_2\left(TT\right)}=0,1.80\%=0,08\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,08.22,4=1,792\left(l\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
Ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{4}>\dfrac{0,08}{5}\), ta được P dư.
Theo PT: \(n_{P\left(pư\right)}=\dfrac{4}{5}n_{O_2}=0,064\left(mol\right)\)
\(\Rightarrow n_{P\left(dư\right)}=0,1-0,064=0,036\left(mol\right)\)
\(\Rightarrow m_{P\left(dư\right)}=0,036.31=1,116\left(g\right)\)
Bạn tham khảo nhé!