Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

13g Zn đko ?
\(n_{Cl_2}=\dfrac{7,1}{71}=0,1\left(mol\right)\\ n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + Cl2 --to--> ZnCl2
LTL: 0,2 > 0,1 => Zn dư
Theo pthh: nZn (pư) = nZnCl2 = nCl2 = 0,1 (mol)
=> nZn (dư) = 0,2 - 0,1 = 0,1 (mol)
PTHH:
\(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\downarrow\)
0,1----------------------------------->0,2
\(ZnCl_2+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2AgCl\downarrow\)
0,1----------------------------------------->0,2
=> mkết tủa = 0,2.108 + 0,2.143,5 = 50,3 (g)

Định hướng tư duy giải
Ta có:
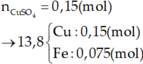
Dễ thấy 6 gam rắn là Fe2O3
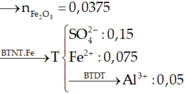
Có Al dư → Phần X phản ứng:
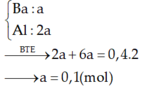
Chú ý: Vì chất tan thu được là Ba(AlO2)2→ tỷ lệ mol Ba : Al phải là 1 : 2
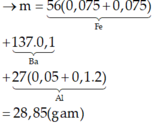

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lý => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol; y = 0,06 mol
=> rắn gồm 0,07 mol MgO và 0,03 mol F e 2 O 3 => m = 7,6 (g)

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư => C u 2 + hết
Giả sử chỉ có Mg phản ứng

Bảo toàn khối lượng gốc kim loại:
![]()
![]()
=> rắn gồm 0,07 mol MgO và 0,03 mol
![]()

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lí => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol => m = 7,6(g)
=> rắn gồm 0,07 mol MgO và 0,03 F e 2 O 3 => m = 7,6 (g)
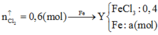
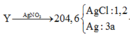



\(n_{Al}=\dfrac{9,45}{27}=0,35\left(mol\right)\\ PTHH:2Al+3Cl_2\underrightarrow{t^o}2AlCl_3\\ \left(mol\right)...0,35\rightarrow........0,35\\ PTHH:AlCl_3+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3AgCl\downarrow\\ \left(mol\right)....0,35\rightarrow..........................1,05\\ m_{AgCl}=1,05.143,5=150,675\left(g\right)\)